
erektion — ejakulation — penis — hoden — endokrinologie — fertilität — genetische aspekte — aging male — varia
Auch bei Männern ist das familiäre Krebsrisiko drastisch erhöht
Nachdem bereits im Altertum aufgefallen war, dass bei den Frauen einiger Familien gehäuft Mammakarzinome auftreten,
gelang es dann in den frühen 90er Jahren des letzten Jahrhunderts mit BRCA1 ein so genanntes Krebs-Suszeptibilitätsgen
zu identifizieren [1]. Kurz darauf kam durch die Entdeckung von BRCA2 ein weiteres Brustkrebs-Gen hinzu [2]. Mutationen
dieser Gene werden über die Keimbahn vererbt und prädestinieren die weiblichen Familienmitglieder für die Entwicklung
von Mamma-, Ovar-, Tuben- und Peritonealkarzinomen. Wie sieht es aber mit den männlichen Familienmitgliedern aus,
die eine BRCA1- oder BRCA2-Mutation ererbt haben? Auch bei ihnen treten verschiedene Krebserkrankungen gehäuft auf,
wobei Träger von BRCA2-Mutationen insbesondere für Brust-, Prostata- und Pankreaskarzinome mit dem höheren Risiko behaftet
sind.
BRCA1/2 kodieren für Zellkern-Proteine
-
Die Proteinprodukte von BRCA1 (1.863 Aminosäuren) und BRCA2 (3.418 Aminosäuren) sind außergewöhnlich groß und
weisen sowohl untereinander als auch mit anderen bekannten Proteinen keinerlei Ähnlichkeiten auf. Interessanterweise
hat man im Erbgut von Hefen, Würmern und Fliegen keine entsprechenden Gene gefunden, sodass sich BRCA1 und BRCA2
während der Evolution offensichtlich erst relativ spät herausgebildet haben. Für Genetiker ist das ein Hinweis
darauf, dass die BRCA-Proteine höchst spezialisierte und möglicherweise gewebsspezifische Funktionen erfüllen.
Die BRCA-Proteine lassen sich im Zellkern nachweisen. Das deutet darauf hin, dass sie mit der DNA in Wechselwirkung
treten. Als weiteres Indiz hierfür, lässt sich ihr zyklisches Auftreten während der Synthese-Phase und der G2-Phase
im Zellzyklus deuten.
-
Bei den Krebs-Suszeptibilitätsgenen unterscheidet man zwischen Pförtnern (gatekeepers) und Hausmeistern (caretakers).
Zu ersteren gehören Gene, deren Proteinprodukte an der Kontrolle des Zellzyklus mitwirken. Fällt ihre Funktion aus,
begünstigt das unkontrollierte Zellteilungen. Die Hausmeister sind insbesondere für die Stabilität des Erbgutes zuständig.
Die BRCA-Proteine sind an grundlegenden zellulären Prozessen beteiligt, deren Ziel es ist, die Stabilität des Erbguts
aufrechtzuerhalten. Hierzu zählen Mechanismen der DNA-Reparatur, der Rekombination, der Überwachung von Kontrollposten im
Zellzyklus und der Transkription. Daraus ist zu folgern, dass den BRCA-Proteinen die Rolle von Tumor-Suppressoren zukommt.
-
Bei den klassischen Tumor-Suppressor-Genen wie z. B. dem Retinoblastom-Gen oder dem Gen für p53 führt erst die Inaktivierung beider
Allele sowohl zur familiären als auch zur sporadischen Krebsentwicklung. Das so genannte Zwei-Treffer-Modell nach Knudsen erklärt
einleuchtend, warum ein über die Keimbahn ererbtes inaktiviertes Allel eines Tumor-Suppressor-Gens, die Anfälligkeit für
Krebserkrankungen drastisch erhöht (Abb.).
|
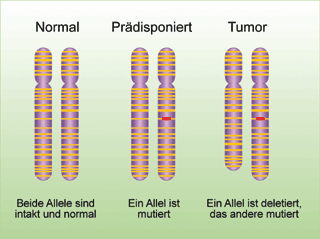
Zwei-Treffer-Hypothese von Knudsen: Tumor-Suppressor-Gene tragen nur zur Krebsentstehung bei, wenn nacheinander
beide Allele inaktiviert werden. Bei Trägern einer ererbten Mutation sind alle Zellen quasi vorgeschädigt. Kommt
in einer Zelle eine sporadische Mutation des intakten Allels wie z.B. durch Deletion hinzu, ist die
Tumor-Suppressor- |
Für BRCA-Mutationen ist die Zwei-Treffer-Hypothese nur insofern zutreffend, als bei familiär erkrankten Personen stets der Verlust beider Allele (Loss of Heterozygosity; LOH) nachgewiesen werden kann. Im Gegensatz dazu findet man bei sporadischen Krebserkrankungen fast immer ein intaktes BRCA1- bzw. BRCA2-Allel.
-
Brustkrebs kommt bei Männern verhältnismäßig selten vor und macht insgesamt weniger als ein Prozent aller Krebserkrankungen
aus. Ist ein Mann allerdings Träger einer BRCA2-Mutation, hat er im Vergleich zur Gesamtbevölkerung ein 80- bis 100-mal
größeres Risiko, an Brustkrebs zu erkranken [3].
Auch für Männer, die ein inaktiviertes BRCA1-Gen über die Keimbahn mitbekommen haben, ist das Brustkrebsrisiko erhöht.
In einer Untersuchung an 483 Trägern einer BRCA1-Mutation aus 147 Familien wurde für betroffene Männer ein 58-fach erhöhtes
Risiko ermittelt, an Brustkrebs zu erkranken [4].
Männer aus BRCA-Familien sollten angewiesen werden auf Veränderungen an der Brust zu achten und sich ähnlich wie Frauen
in Abständen selbst abzutasten. Bei Männern wird ein Brustkrebs meist erst in einem fortgeschritteneren Stadium diagnostiziert
als bei Frauen. Die Prognose ist dementsprechend schlechter.
-
Die Träger einer BRCA1-Mutation haben nach neueren Untersuchungen ein relatives Risiko von 1,8, unter 65 Jahren an
einem Prostatakarzinom zu erkranken. Danach gleicht sich das Risiko dem in der Gesamtbevölkerung an [5].
Der Zusammenhang zwischen einem erhöhten Prostatakarzinom-Risiko und BRCA2-Mutationen ist deutlicher ausgeprägt als
für BRCA1-Mutationen. Das relative Prostatakarzinomrisiko für Träger einer BRCA2-Mutation ist nach einer großen
diesbezüglichen Studie bis zum 65. Lebensjahr immerhin 7,33 [6].
-
Die beiden Brustkrebsgene werden ubiquitär exprimiert, sodass sich bei ihrer Inaktivierung in zahlreichen Geweben bzw.
Organen Karzinome entwickeln können. Zwar ist das Brust- und Ovarialkrebsrisiko bei Trägerinnen von BRCA1-Mutanten exzeptionell
hoch, doch kommen insbesondere auch Kolon-, Pankreas- und Magenkarzinome gehäuft vor. Für männliche Träger einer BRCA1-Mutation
wurde ein mehr als doppelt so hohes Krebsrisiko wie für Trägerinnen einer BRCA1-Mutation ermittelt (ohne Brust- und Ovarialkakarzinome).
Bei Pankreaskarzinomen besteht eine stärker ausgeprägte Beziehung zu BRCA2- als zu BRCA1-Mutationen. Träger einer ererbten BRCA2-Mutation haben ein etwa 3,5-faches Risiko, an einem Pankreaskarzinom zu erkranken, als der Rest der Bevölkerung [6]. Zudem tritt die Erkrankung meist bereits in jüngeren Jahren auf als bei den sporadischen Pankreaskarzinomen. Das erhöhte Pankreaskarzinomrisiko für Träger einer BRCA2-Mutation wurde auch durch Untersuchungen in Familien mit mehr als einem erkrankten Verwandten ersten Grades bestätigt. Bei 12% der erkrankten Personen wurde eine solche Mutation gefunden [7].
Verschiedene Quellen geben das relative Risiko, ein Kolonkarzinom zu entwickeln, für Träger einer BRCA1-Mutatiom mit zwei an [4, 5].
Hingegen besteht nach Untersuchunges des Breast Cancer Linkage Consortiums für Träger einer BRCA2-Mutation kein erhöhtes Kolonkarzinomrisiko [6].
Reviews:
Literatur:
[1] Miki Y, Swensen J, Shattuck-Eidens D, et al. 1994.
A strong candidate for the breast and ovarian cancer susceptibility gene BRCA1. Science 266:66-71.
[2] Wooster R, Bignell G, Lancaster J, et al. 1995.
Identification of the breast cancer susceptibility gene BRCA2. Nature 378:789-792.
[3] Thompson D, Easton DF. 2001.
Variation in cancer risks, by mutation position, in BRCA2 mutation carriers. Am J Hum Genet 68:410-419.
[4] Brose MS, Rebbeck TR, Calzone KA, et al. 2002.
Cancer risk estimates for BRCA1 mutation carriers identified in a risk evaluation program. J Natl Cancer Inst 94:1365-1372.
[5] Thompson D, Easton DF. 2002.
Cancer incidence in BRCA1 mutation carriers. J Natl Cancer Inst 94:1358-1365.
[6] The Breast Cancer Linkage Consortium. 1999.
Cancer risks in BRCA2 mutation carriers. J Natl Cancer Inst 91:1310-1316.
[7] Hahn SA, Greenhalf B, Ellis I, et al. 2003.
BRCA2 germline mutations in familial pancreatic carcinoma. J Natl Cancer Inst 95:214-221.
[1] Liede A, Karlan BY, Narod SA. 2004.
Cancer risk for male carriers of germline mutations in BRCA1 or BRCA2: a review of the literature. J Clin Oncol 22:735-742.
[2] Venkitaraman AR. 2002.
Cancer susceptibility and the functions of BRCA1 and BRCA2. Cell 108:171-182.
[3] Scully R. 2001. Interactions between BRCA proteins and DNA structure. Exp Cell Res 264:67-73.
© 2003-2026 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz
