
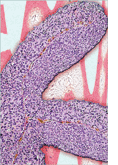
Höchst variable Risiken für Rezidive und Progression
Das Urothelkarzinom ist der bei weitem häufigste Tumor der Harnblase. Das Erkrankungsrisiko von Männern ist bis
zu fünfmal höher als das von Frauen. Eine Reihe von Befunden deutet auf eine hormonelle Komponente in der Ätiologie
und Progression des Urothelkarzinoms hin. Bei der Diagnosestellung ist der Krebs in 70% bis 80% der Fälle noch auf
das Epithel beschränkt. Diese pTa-Tumoren werden nach der aktuellen WHO-Klassifikation gemäß ihrer klinischen,
histopathologischen und molekularen Eigenschaften in niedrig- und hoch-maligne papilläre Tumoren eingeteilt. Das
Carcinoma in situ (Cis) ist auch bei einer Ausdehnung auf nur wenige Zellen mit einem hohen Malignitätspotenzial
behaftet. Die Instillationstherapie mit Bacillus Calmette-Guérin ist zumindest bei hoch-malignen nicht-muskelinvasiven
Urothelkarzinomen einschließlich Cis als Standardtherapie etabliert. Darüber hinaus kommen beim Blasenkarzinom sowohl
intravesikale und systemische Chemotherapien zur Anwendung. Aufgrund der hohen Malignität zahlreicher Blasentumoren
stellt die radikale Zystektomie vielfach nicht nur bei lokal fortgeschrittenen Tumoren die geeignetste Therapieform dar.
Epidemiologie des Urothelkarzinoms der Harnblase
-
Das Harnblasenkarzinom gehört zu den häufigsten Krebserkrankungen und steht beim Mann nach dem Prostata-, Lungen- und
Dickdarmkarzinom an vierter Stelle aller Malignome. In ca. 95% der Fälle handelt es sich um epitheliale Tumoren, von
denen wiederum mehr als 90% Urothelkarzinome sind.
Tatsache ist, dass Männer von Krebserkrankungen der Harnblase bis zu fünfmal häufiger betroffen sind als Frauen. Als Erklärung hierfür wird oft eine berufliche Exposition mit Karzinogenen angeführt. Verschiedene alternative Hypothesen berücksichtigen in erster Linie genetische, anatomische, hormonelle, sozio-ökonomische und Umweltfaktoren.
Bei Frauen ist ein Harnblasenkarzinom bei der Diagnosestellung häufiger als bei Männern bereits in einem fortgeschrittenen
Stadium. Demzufolge sterben relativ gesehen weniger Männer als Frauen an Blasenkrebs. Ferner steht weibliches Geschlecht
im Zusammenhang mit einem schlechteren Ergebnis nach Zystektomie [1].
-
Das lokalisierte Blasenkarzinom wird in nicht-muskelinvasive (Ta, T1, Cis) und muskelinvasive (T2a-T4b) Krankheitsstadien
untergliedert. Entsprechend der aktuellen WHO-Klassifikation wird bei nicht-invasiven Urothelkarzinomen (Ta) zwischen low
grade- und high grade-Tumoren unterschieden (Tabelle). Die Klassifizierung dieser papillären Urotheltumoren (pTa) erfolgt
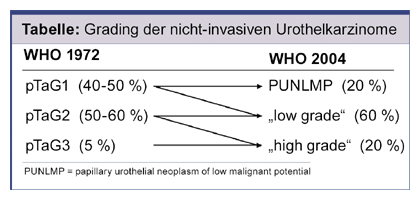 nach zunehmendem Atypiegrad in ein non-invasive papillary urothelial neoplasm of low malignant potential (PUNLMP), ein nicht
invasives papilläres Urothelkarzinom low grade und ein nicht invasives papilläres Urothelkarzinom high grade. Bei PUNLMP
und nicht invasiven papillären Urothelkarzinomen low grade sind die genetische Instabilität und damit Epithelatypien nur
gering ausgeprägt. Das Risiko der Progression wird als niedrig (<5%) eingestuft. Die genetisch instabilen high grade-Tumoren
weisen hingegen deutliche Epithelatypien auf. Aus ihnen entwickeln sich mit höherer Wahrscheinlichkeit invasive Tumoren.
nach zunehmendem Atypiegrad in ein non-invasive papillary urothelial neoplasm of low malignant potential (PUNLMP), ein nicht
invasives papilläres Urothelkarzinom low grade und ein nicht invasives papilläres Urothelkarzinom high grade. Bei PUNLMP
und nicht invasiven papillären Urothelkarzinomen low grade sind die genetische Instabilität und damit Epithelatypien nur
gering ausgeprägt. Das Risiko der Progression wird als niedrig (<5%) eingestuft. Die genetisch instabilen high grade-Tumoren
weisen hingegen deutliche Epithelatypien auf. Aus ihnen entwickeln sich mit höherer Wahrscheinlichkeit invasive Tumoren.Mit der Einführung einer Subklasse nicht-invasiver, hoch-maligner (high grade) Urothelkarzinome wird zugleich eine neue, in ihrer Inzidenz nicht unerhebliche Klasse von Hochrisiko-
Als flache intraepitheliale Läsionen werden das Carcinoma in situ (Cis) mit high grade und die Dysplasie als low grade klassifiziert.
Patienten mit einem pT1-Blasentumor werden über die Invasion des subepithelialen Bindegewebes (Lamina propria) definiert. Obwohl T1-Tumoren als oberflächlicher Blasenkrebs klassifiziert wird, kommen solche Tumoren in unmittelbaren Kontakt mit den subepithelialen Blut- und Lymphgefäßen. Bei Patienten mit T1-Übergangszelltumoren, die sich einer radikalen Zystektomie unterziehen, finden sich nicht selten Metastasen in den regionalen Lymphknoten. Gen-Expressionsprofile lassen eine weitgehende Übereinstimmung mit muskelinvasiven pT2-Tumoren erkennen [2].
In der molekularen Pathogenese und Prognose des Urothelkarzinoms lassen sich zwei differente Entwicklungswege unterscheiden [3, 4]: In oberflächlichen Blasentumoren treten gain-of function-Mutationen der Onkoproteine RAS, Fibroblasten-Wachstumsfaktor-Rezeptor-3 und Phosphatidyinositol-3-Kinase wie auch Deletionen im langen Arm von Chromosom 9 (9q) häufig auf. Andererseits finden sich beim Cis und in invasiven Tumoren loss-of-function-Mutationen der Tumorsuppressorproteine p53, Retinoblastom und PTEN.
-
Eine mikropapillare Morphologie kommt in Neoplasien verschiedener Organsysteme vor. Solche Tumoren darunter auch Urothelkarzinome
mit mikropa-pillären Merkmalen sind verhältnismäßig selten. Sie entwickeln ungeachtet der Herkunft des Ursprungstumors überwiegend
ein sehr aggresives Verhalten. Insgesamt haben mikropapilläre Urothelkarzinome eine sehr schlechte Prognose, auch wenn einige Studien
berichten, dass das Krankheitsergebnis durch frühzeitige radikale Zystektomie verbessert werden könne. Die Tumoren sprechen aller
Wahrscheinlichkeit nach nicht auf eine als Zweitlinientherapie angewandte Chemotherapie an [5].
Lopez-Beltram et. al. (2010) berichten über 13 Fälle von invasiven mikropapillären Varianten des Urothelkarzinoms der Harnblase.
Die mikropapilläre Komponente in den Tumorproben variierte anteilmäßig von 50% bis zu 100%. Alle Patienten hatten Blasenkrebs im
fortgeschrittenen Stadium (>pT2) und bei 8 wurden Metastasen in Lymphknoten vorgefunden. Immunhistochemisch wurden sowohl in den
mikropapillären Anteilen als auch in angrenzenden herkömmlichen Urothelkarzinomen positive Färbergebnisse für MUC1 und 2, Zytokeratin 7,
PTEN, p53 sowie Ki-67 erhalten. In einigen Fällen ließen sich auch HER2, Uroplakin, Zytokeratin 20, CA125 und p16 nachweisen. Der
Immunophänotyp des mikropapillären Karzinoms spricht somit für einen urothelialen Ursprung [6].
-
Bei der Suche nach möglichen Erklärungen für die unterschiedliche Inzidenz wie auch für die differenten Eigenschaften des Urothelkarzinoms
der Harnblase bei Männern und Frauen wurden Sexualsteroidhormone und deren Rezeptoren in der Harnblase untersucht. Hierbei deuten
tierexperimentelle Befunde auf eine Rolle des Androgen/Androgenrezeptor-Systems beim Blasenkrebs hin. Wildtyp- und so genannte
Androgenrezeptor-Knockout (ARKO)-Mäuse wurden mit dem Blasenkrebs auslösenden N-Butyl-N-(4-hydroxybutyl)nitrosamin behandelt. Bei mehr
als 92% der männlichen und 42 % der weiblichen Wildtyp-Mäuse entwickelte sich Blasenkrebs, während das bei keiner männlichen oder weiblichen
ARKO-Maus der Fall war [7].
Androgenrezeptoren wurden beim Menschen im normalen Blasenepithel wie auch in Blasentumoren von Männern und Frauen nachgewiesen. In Zelllinien aus menschlichen Übergangszell-Karzinomen ließen sich durch Behandlung mit kleinmolekularer interferierender RNA (siRNA) gegen den Androgenrezeptor die Proliferationsraten wie auch die Migrationskapazität der Zellen deutlich senken und die Apoptoseraten signifikant steigern. Zugleich wurde eine Erniedrigung der Expression von Wachstums- und Metastasierungs-bezogenen Genen wie Cyclin D1, Bcl-xL und der Matrix-Metallopeptidase-9 mittels quantitativer Reverse-Transkriptase-Polymerasekettenreaktion festgestellt. Ähnliche Ergebnisse lieferte die Behandlung von Urotheltumor-tragenden Nacktmäusen bei Behandlung mit siRNA gegen den Androgenrezeptor. Die Untersucher glauben, dass die Herunterregulierung der Androgenrezeptor-Expression bei Blasenkrebs als therapeutisches Ziel genutzt werden könnte [8].
-
Harnblasenkarzinome befinden sich bei der Diagnosestellung weit überwiegend noch in einem nicht-invasiven Stadium (pTa). In weniger als 20% der
Fälle erkranken Männer vor Erreichen des 60. Lebensjahres.
In der Therapie des nicht-invasiven Urothelkarzinoms der Harnblase kommen operative (blasenerhaltend und nicht-blasenerhaltend; partielle
Zystektomien werden nur in Ausnahmefällen durchgeführt) wie auch konservative Therapieverfahren zur Anwendung.
Transurethrale Resektion (TUR)
Bei der transurethralen Resektion (TUR) werden beim oberflächlichen Harnblasenkarzinom zugleich diagnostische und kurative Ziele verfolgt.
Hierbei gilt es das korrekte Tumorstadium zu erfassen und alle sichtbaren Läsionen vollständig zu entfernen.
Bei pT1-Tumoren und bei positiven Randbiopsien ist eine Nachresektion nach 1-6 Wochen erforderlich. Diese Maßnahme empfiehlt sich auch bei
Ta/T1-high grade-Karzinomen. Weiterhin ist eine Nachresektion bei Patienten angezeigt, in deren pathologischem Präparat keine Muskulatur
zu erkennen war [10].
Radikale Zystektomie
Auch bei Hochrisiko-Blasenkrebs der Stadien Ta, T1 und Cis wird von der EAU eine Empfehlung für die radikale Zystektomie als alternative
Therapie bei Rezidiven nach intravesikaler Behandlung mit Bacillus Calmette-Guérin ausgesprochen [11].
Strahlenbehandlung im Rahmen multimodaler Therapien
In einer aktuellen Übersichtsarbeit berichten Kotwal und Munro (2010) über Ergebnisse verschiedener Studien der letzten Jahre, in denenen
Patienten mit Hochrisiko-pT1-Tumoren oder organbegrenztem muskelinvasivem Blasenkrebs im Rahmen einer multimodalen Therapie meist in
Verbindung mit endoskopischer Tumorresektion und einer Chemotherapie bestrahlt wurden. Solche Prüfungen waren überwiegend in einzelnen
Institutionen durchgeführt worden. Sie zeigten durchweg befriedigende Resultate hinsichtlich des krankheitsfreien Überlebens und der lokalen
Kontrolle des Tumors [12].
Instillationstherapie mit Bacillus Calmette-Guérin
Bereits in den späten 1980er Jahren zeigte sich, dass die Verabreichung von Bacillus Calmette-Guérin (attenuierte Tuberkuloseerreger) in die
Harnblase eine effektive Form der Immuntherapie dieser Krankheit darstellt. Auch wenn die exakten Mechanismen noch nicht aufgeklärt sind, wird
davon ausgegangen, dass Bacillus Calmette-Guérin offenbar eine lokale Immunreaktion gegen den Tumor hervorruft.
Instillation mit Gemcitabin nach Bacillus Calmette-Guérin
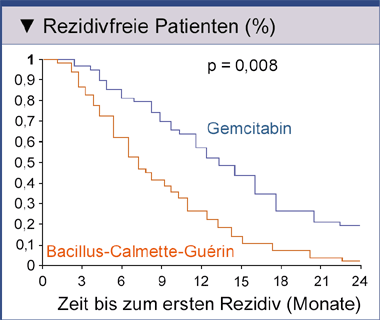
Patienten mit einem nicht-muskelinvasivem high risk-Urothelkarzinom der Harnblase, bei denen nach dem Fehlschlagen einer Instillationstherapie mit Bacillus Calmette-Guérin eine radikale Zystektomie indiziert gewesen wäre, aber aus verschiedenen Gründen nicht durchgeführt werden konnte, wurden randomisiert nochmals mit Bacillus Calmette-Guérin oder intravesikal mit Gemcitabin behandelt. Die Kaplan-Meier-Kurven für rezidivfreies Überleben zeigen einen deutlich günstigeren Verlauf für den Gemcitabin-Arm (Abb. 1). In beiden Behandlungsgruppen traten relativ wenige schwere (Grad 3) Nebenwirkungen auf [14].
|
Abb. 1: Kaplan-Meier-Kurven für rezidivfreies Überleben bei Patienten mit einem nicht-muskelinvasivem high risk-Urothelkarzinom der Harnblase, bei denen nach dem Fehlschlagen einer Instillationstherapie mit Bacillus Calmette-Guérin eine radikale Zystektomie indiziert gewesen wäre, aber aus verschiedenen Gründen nicht durchgeführt werden konnte, und die randomisiert nochmals mit Bacillus Calmette-Guérin oder intravesikal mit Gemcitabin behandelt wurden (nach Di Lorenzo G, et al. 2010). |
Intravesikales Gemcitabin und Mitomycin im Vergleich
Je nach Untersuchung sprechen 30% bis 40% der Patienten mit oberflächlichem Blasenkrebs auf eine Behandlung mit Bacillus Calmette-Guérin nicht (hinreichend) an, und von denen, die initial ansprechen, erleiden 45% innerhalb von fünf Jahren ein Rezidiv.
Die Patienten in beiden Armen, die nach einem initialen Behandlungskurs ohne Rezidiv blieben, setzten die Therapie aus zehn monatlichen Behandlungen im ersten Jahr fort.
Von den 120 randomisierten Patienten (60/60; 47/46 Männer) konnten die Daten von 55 Patienten im Mitomycin-Arm und 54 Patienten im Gemcitabin-Arm ausgewertet werden. Die mittlere Nachbeobachtungszeit betrug in beiden Armen 36 Monate.
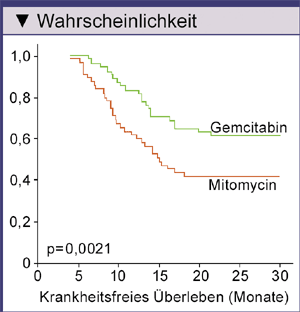
Im Gemcitabin-Arm blieben 39 von 54 Patienten (72%) und im Mitomycin-Arm 33 von 55 Patienten (62%) ohne Rezidiv (Abb. 2).
|
Abb. 2: Kaplan-Meier-Kurven für krankheitsfreies Überleben seit Studieneintritt bei Patienten mit oberflächlichem Blasenkrebs Grad 3 (nach Addeo R, et al. 2010). |
Bei den Patienten mit einem Rezidiv unter der Behandlung waren 10 Tumoren im Mitomycin-Arm und 6 Tumoren im Gemcitabin-Arm auch im Stadium progredient geworden. Eine chemische Zystitis trat im Mitomycin-Arm signifikant häufiger auf als im Gemcitabin-Arm (p=0,012).
Gemcitabin erwies sich rezidiviertem oberflächlichem Blasenkrebs gegenüber Mitomycin als wirksamer und besser verträglich. Ihm wird die Rolle
eines Kandidaten für die Instillationstherapie bei Patienten mit refraktärem Übergangszellkarzinom beigemessen.
Literatur:
[1] Shariat SF, Sfakianos JP, Droller MJ, et al. 2009. The effect of age and gender on bladder cancer: a critical review of the literature. BJU Int 105:300-308.
[2] Wild PJ, Herr A, Wissmann C, et al. 2005. Gene expression profiling of progressive papillary noninvasive carcinomas of the urinary bladder. Clin Cancer Res 11:4415-4429.
[3] Hofstädter F, 2008. Urothelkarzinom. Lernt die Pathologie von der Molekularpathologie? Pathologe 29(Suppl 2):145-148.
[4] Castillo-Martin M, Domingo-Domenech J, et al. 2010. Molecular pathways of urothelial development and bladder tumorigenesis. Urol Oncol 28:401-408.
[5] Watts KE, Hansel DE, 2010. Emerging concepts in micropapillary urothelial carcinoma. Adv Anat Pathol 17:182-186.
[6] Lopez-Beltran A, Montironi R, Blanca A, Cheng L, 2010. Invasive micropapillary urothelial carcinoma of the bladder. Hum Pathol 41:1159-1164.
[7] Miyamoto H, Yang Z, Chen Y-T, et al. 2007. Promotion of bladder cancer development and progression by androgen receptor signals. J Natl Cancer Inst 99:558-568.
[8] Wua J-T, Han BM, Yu S-Q, et al. 2010. Androgen Receptor is a Potential Therapeutic Target for Bladder Cancer. Urology 75:820-827.
[9] Boorjian S, Ugras S, Mongan NP, et al. 2004. Androgen receptor expression is inversely correlated with pathologic tumor stage in bladder Cancer. Urology 64:383-388.
[10] vom Dorp F, Kausch I, Jocham D, 2007. Diagnostik und Therapie des nichtinvasiven Harnblasenkarzinoms. Dtsch Arztebl 104:A 797-A 802.
[11] Babjuk M, Oesterlinck W, Sylvester R, et al. 2008. EAU guidelines on nonmuscle-invasive urothelial carcinoma of the bladder. Eur Urol 54:303-314.
[12] Kotwal S, Munro N, 2010. Radiotherapy in localized bladder cancer: what is the evidence? Curr Opin Urol 20:426-431.
[13] Gontero P, Bohle A, Malmstrom PU, et al. 2010. The role of bacillus Calmette-Guérin in the treatment of non-muscle-invasive bladder cancer. Eur Urol 57:410-429.
[14] Di Lorenzo G, Perdonà S, Damiano R, et al. 2010. Gemcitabine versus bacille Calmette-Guérinafter initial bacille Calmette-Guérin failure in non-muscle-invasive bladder cancer. Cancer 116:1893-1900.
[15] Addeo R, Caraglia M, Bellini S, et al. 2010. Randomized phase III trial on gemcitabine versus mitomycin in recurrent superficial bladder cancer: evaluation of efficacy and tolerance. J Clin Oncol 28:543-548.
© 2003-2026 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz
