
Testosteronsubstitution bei jüngeren Krebsüberlebenden
Hintergrund
Zielsetzung
Teilnehmer und Methoden
Die Gruppen waren nach Alter, Körpergröße, BMI, Testosteron-Status, Krebsart und Zeit seit der Krebsbehandlung recht gut ausgewogen.
| ||||
|
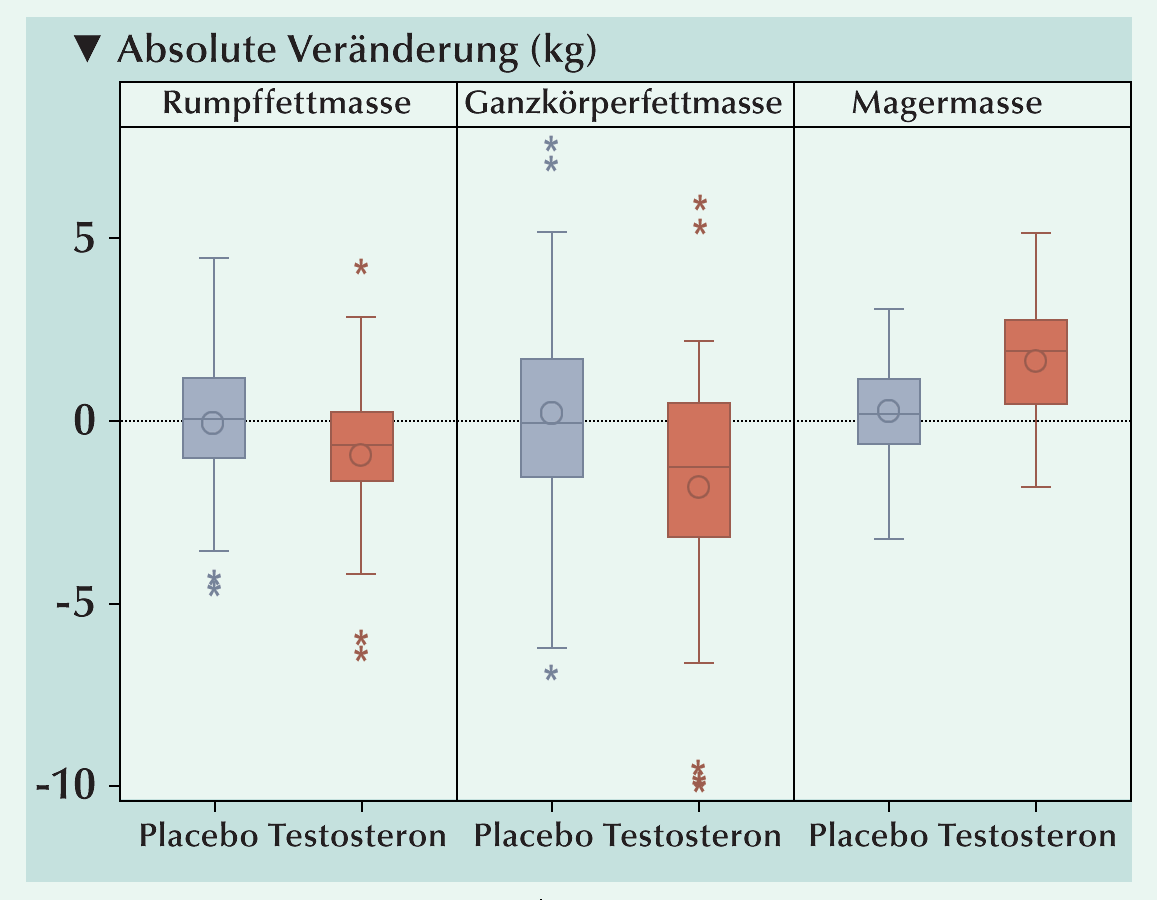
Abb.: Veränderungen der Stammfettmasse, der Gesamtkörper-Fettmasse und der Gesamtkörper-Magermasse
nach in der Testosteron- und Placebo-Gruppe nach 26 Wochen. Die Boxen stellen den Interquartilbereich, die Kreise
das Mittel und die Linien in den Boxen den Median der Veränderungen ausschließlich der Ausreißer (Sternchen) dar. | ||||
Primäre Endpunkte
Nach 26 Wochen Testosteron-Behandlung wurde eine statistisch signifikante Abnahme der
Stammfettmasse registriert (Abb.). Der Behandlungseffekt belief sich auf -0,9 kg (p = 0,007).
In der Behandlungsgruppe betrug der Verlust an Stammfettmasse bei jedem vierten Mann mehr als 1,5 kg.
Der Testosteron-Ausgleich war nach 26 Behandlungswochen nicht mit der Chance auf einen vollkommenen
Score des SF36 für körperliche Funktionsfähigkeit assoziiert
(Odds Ratio = 0,77, p = 0,58).
Sekundäre Endpunkte
Die Testosteron-Behandlung stand auch mit einer Abnahme der Gesamtkörper-Fettmasse (-1,8 kg,
p = 0,0016) und einer Zunahme der Gesamtkörper-Magermasse (1,5 kg, p < 0,001) (Abb.)
im Zusammenhang. Die Behandlung war mit günstigen Veränderungen des Verhältnisses Nüchtern-Insulinspiegel:Glukosespiegel,
des Nüchtern-Lipidspiegels, der Knochendichte, des BMI, des Bauchumfangs, dem SF36-Score, der Fatigue
nach dem Functional Assessment of Chronic Illness Therapy und der Selbstachtung gemäß Rosenberg Self-Esteem Fragebogen.
assoziiert.
❏ Der Nutzen einer Testosteronbehandlung kommt womöglich insbesondere jenen Männern mit erhöhter Stammfettmasse zugute.
❏ Bei diesen Patienten wird die Testosteronsubstitution im Zusammenhang mit weiteren Interventionen zur Verbesserung der Körperzusammensetzung angeregt.
Walsh JS, Marshall H, Smith IL, et al. 2019. Testosterone replacement in young male cancer survivors: A 6-month double-blind randomised placebo-controlled trial PLOS Medicine | https://doi.org/10.1371/journal.pmed.1002960
© 2003-2025 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz


