
Reaktionen des Muskels bei durch Androgendeprivation induzierter Sarkopenie
Hintergrund
Die Androgendeprivationstherapie (ADT) gehört zu den standardmäßigen Behandlungsmethoden
bei lokal fortgeschrittenem und metastasiertem Prostatakrebs. Dabei kommt es unter anderem zum
Verlust an Muskelmasse. Deren Bestand wird durch ein dynamisches Gleichgewicht zwischen
Muskelprotein-Synthese und den -Abbau aufrechterhalten. Die Regulierung dieser Prozesse erfolgt
über komplexe Signalwege, in denen Testosteron eine Schlüsselrolle als Modulator einnimmt. Das
aktuelle Verständnis der Mechanismen zur Regulierung von Muskelmasse und Muskelfunktion durch
Androgene wurde in einer Übersicht herausgestellt [1].
Androgene sind ein bestimmender Faktor für den Aufbau und den Erhalt von Skelettmuskulatur.
Dementsprechend kommt es bei Androgenmangel zu Sarkopenie, worunter allgemein der Abbau von Muskulatur
und weiterer fettfreier Körpermasse zusammengefasst wird. Unter einer ADT machen sich bei Männern auf
makroskopischer Ebene Sarkopenie und Adipositas bemerkbar. Dabei steht einer ca. 2 bis 4%igen Abnahme
der fettfreien Substanz die um ca. 10 bis 20% anwachsende Masse des Körperfetts gegenüber [2].
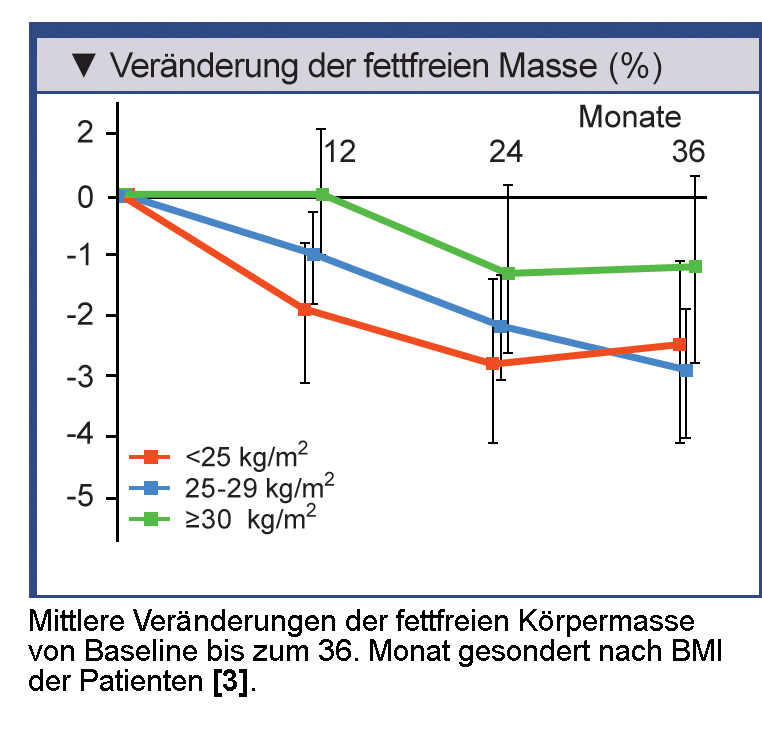 Von der Abnahme fettfreier Körpermasse sind insbesondere Männer 70 Jahre mit normolem oder mäßig
erhöhtem Körpergewicht betroffen (Abb.), [3].
Von der Abnahme fettfreier Körpermasse sind insbesondere Männer 70 Jahre mit normolem oder mäßig
erhöhtem Körpergewicht betroffen (Abb.), [3].
Aktivierung der Satellitenzellen  Von der Abnahme fettfreier Körpermasse sind insbesondere Männer 70 Jahre mit normolem oder mäßig
erhöhtem Körpergewicht betroffen (Abb.), [3].
Von der Abnahme fettfreier Körpermasse sind insbesondere Männer 70 Jahre mit normolem oder mäßig
erhöhtem Körpergewicht betroffen (Abb.), [3].
Die Muskelmasse kann durch Testosteron-induzierte Aktivierung der Satellitenzellen anwachsen.
Auch wenn der genaue Einfluss auf Proliferation und Differenzierung der Satellitenzellen noch nicht
vollstädig aufgeklärt ist, wird davon ausgegangen, dass Testosteron als Modulator der primären
Differenzierung (Zelldetermination) fungiert. Dabei wird die adipöse Differenzierung zugunsten
der myogenen Differenzierung inhibiert. Bei Androgendeprivation tritt der gegenteilige Effekt
ein und führt zu Sarkopenie und Adipositas.
Inhibierung der Myostatin-Aktivität
Anabole Effekte des Testosterons können durch Supprimierung der Expression und/oder
Aktivität von Myostatin zustandekommen. Trotz einiger Unsicherheiten über den genauen Mechanismus,
wird der abnehmenden Inhibition des Myostatins bei dem durch Androgenmangel bewirkten Muskelschwund
erhebliche Bedeutung beigemessen.
Stimulierung der GH/IGF1-Achse
Die Rolle von Myostatin als wesentlicher Modulator des Muskelschwundes bei Androgenmangel
wurde durch die Wirksamkeit eines Myostatin-Inhibitors bei ADT-Patienten mit nicht-metastasiertem
Prostatakrebs unterstrichen.
Die Androgen-induzierte Stimulierung der Wachstumshormon/insulinähnlicher Wachstumsfaktor
(IG/IGF1)-Achse aktiviert den anabolen Akt/mTOR-Reaktionsweg. Als wahrscheinlicher Mechanismus,
der für den Verlust an Muskelmasse unter ADT favorisiert wird, kommt die Verringerung des
IGF1-Spiegels und daraus resultierende verminderte Akt/mTOR-stimulierte anabole Aktivität
in Frage. IGF1 ist für die Vermittlung anaboler Testoateron-Effekte bedeutsam. Insbesondere
die Proliferation und Differenzierung der Myoblasten wird angeregt.
Klinische Belange
Die Aufklärung der Reaktionswege und ihrer Regulierung soll einerseits zur Entwicklung
pharmaueutischer Präparate führen, mit denen sich die Muskelfunktion vor ... schützen lässt.
Andererseits kann sie dazu beitragen, körperliche Übungen der gegenwärtig einzigen verfügbaren
Therapie bei ADT-verursachtem Abbau von Muskelmasse und Muskelkraft auf Trainingseinheiten
konzentrieren zu können, die in erster Linie die Verbesserung der Muskelfunktion und weniger
den Muskelzuwachs begünstigen.
Schlussfolgerungen
Der Muskel ist ein Gewebe, das sehr ausgeprägt auf Testosteron anspricht. An den komplexen myogenen
Effekten des Sexualhormons, ist eine Reihe zellulärer Signal- und Reaktionwege involviert. Die Aktivierung
und Differenzierung der Satellitenzellen, die Stimulierung der GH/IGF1-Achse und die Inhibierung des
Myostatins spielen bei ADT-bewirkter Sarkopenie eine zentrale Rolle. Hierin werden Ansatzpunkte für die
Entwicklung pharmazeutischer Präparate gesehen, mit denen die Muskulatue bei Männern unter einer ADT besser
geschützt werden kann.
Literatur:
[1] de Rooy C, Grossmann M, Zajac JD, Cheung AS, 2016. Targeting muscle signaling pathways to minimize adverse effects of androgen deprivation. Endocr Relat Cancer 23:R15-R26.
[2] Cheung AS, Zajac JD, Grossmann M, 2014. Muscle and bone effects of androgen deprivation therapy: current and emerging therapies. Endocr Relat Cancer 21:R371-R394.
[3] Smith MR, Saad F, Egerdie B, et al. 2012. Sarcopenia during androgen-deprivation therapy for prostate cancer. J Clin Oncol 30:3271-3276.
[1] de Rooy C, Grossmann M, Zajac JD, Cheung AS, 2016. Targeting muscle signaling pathways to minimize adverse effects of androgen deprivation. Endocr Relat Cancer 23:R15-R26.
[2] Cheung AS, Zajac JD, Grossmann M, 2014. Muscle and bone effects of androgen deprivation therapy: current and emerging therapies. Endocr Relat Cancer 21:R371-R394.
[3] Smith MR, Saad F, Egerdie B, et al. 2012. Sarcopenia during androgen-deprivation therapy for prostate cancer. J Clin Oncol 30:3271-3276.
© 2003-2025 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz


