
Neue Hoffnungsträger für Diagnose, Prognose und Therapie
Eine Reihe von miRNA mit Prostatakrebs-spezifischer Expression und unterschiedlichen Targets wurde identifiziert. In In-vitro- und in Tierexperimenten wurde die Beeinflussung von Prostatakrebswachstum durch Wiederherstellung der Funktion von miRNA bereits erfolgreich getestet. Andererseits dürfte das Einbringen von miRNA, miRNA-Agonisten oder miRNA-Antagonisten in Prostatakrebszellen am Patienten noch eine erhebliche Hürde auf dem Weg zu erfolgreichen miRNA-basierten Therapiestrategien darstellen.
Jede Menge Schrott glaubte man im menschlichen Erbgut gefunden zu haben, nachdem die Sequenzierung der genomischen DNA im Rahmen des Humangenomprojekts zur Jahrtausendwende für abgeschlossen erklärt wurde. Denn den mindestens 98 Prozent der DNA, die sich zwischen den Protein-kodierenden Genen befindet, kam keine erkennbare Funktion zu. Das hat sich in jüngerer Zeit so grundlegend geändert, dass der Schrott im Jahr 2006 sogar mit dem Nobelpreis vergoldet wurde. Die Laureaten Craig Mello und Andrew Fire, wie auch eine Reihe weiterer beteiligter Forscher, hatten erkannt, dass eine Vielzahl kleiner RNA-Moleküle (mikroRNA) in zahlreiche biologische Prozesse regulatorisch eingreift. Sie wechselwirken auf sequenzspezifische Weise mit Messenger (m)RNA und regulieren die Gen-Expression post-transkriptionell. Dieser Mechanismus, der auch als RNA-Interferenz bezeichnet wird, lässt sich experimentell heute schon dazu nutzen, Gene gezielt stumm zu schalten. Die Schlüsselrolle der mikroRNA im Rahmen tumorassoziierter zellulärer Prozesse macht sie zu viel versprechenden Kandidaten für die Entwicklung diagnostischer und prognostischer Biomarker wie auch als Therapie-Targets
Gene, die nur als RNA ausgeprägt werden
-
Ist von Genen die Rede, werden damit zumeist DNA-Abschnitte gemeint, die in RNA umgeschrieben und schließlich als Proteine
ausgeprägt (exprimiert) werden. Doch beim Menschen machen die schätzungsweise etwa 30.000 derartiger Gene nur einen verschwindend
kleinen Teil der gesamten Erbsubstanz von ca. drei Milliarden Basenpaaren aus. Den überwiegenden Teil der DNA qualifizierte
man etwas voreilig als evolutionären Schrott ab und warf ihn wie sich Molekularbiologen und Genetiker auszudrücken
pflegen kurzerhand in den Mülleimer. Im Hinterkopf rumorte aber immer die Frage, warum diese so genannte Junk-DNA dennoch
großenteils in RNA umgeschrieben, d.h. in hohem Maße transkribiert wird.
-
Von den Sequenz-spezifischen post-transkriptionellen Regulatoren der Gen-Expression wurden zwei Klassen kleiner RNA-Moleküle
entdeckt: die small interfering RNA (siRNA) und die mikroRNA (miRNA). Die Biosynthese beider RNA-Formen, ihr Einbau in einen
RNA-Proteinkomplex, und dessen Fähigkeit die Bildung bestimmter Proteinprodukte auf mRNA-Ebene herunterzuregulieren sind in
Abbildung 1 dargestellt. Obwohl miRNA und siRNA unterschiedlichen Vorläufermolekülen entstammen, weisen sie
identische biochemische Merkmale auf.
|
|
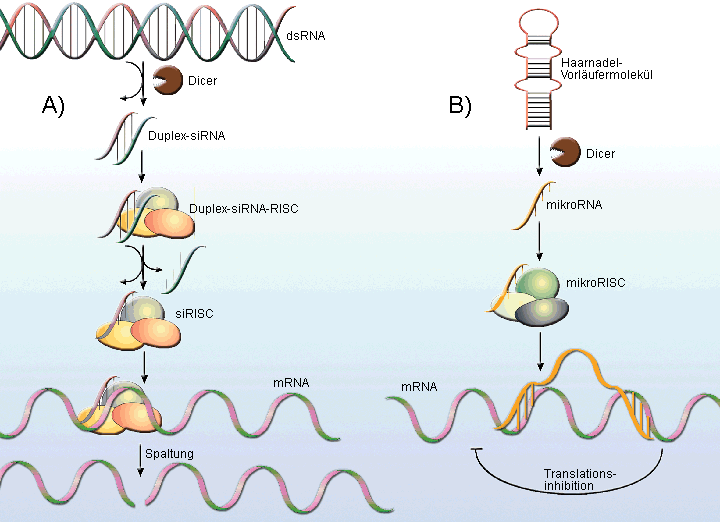
Abb. 1: Wege zur RNA-Interferenz: A) siRNA-Interferenz Lange doppelsträngige (ds)RNA wird durch einen Würfelschneider (Dicer) zur Duplex siRNA gespalten und in einen RNA inducing silencing complex (RISC) inkorporiert. Es schließt sich das Entwinden der Duplex-siRNA an. Durch den einsträngigen Antisense-siRNA-Strang wird der RISC mit der komplementären messenger (m)RNA hybridisiert. Es resultiert die endonukleolytische Spaltung der mRNA.
B) mikro RNA-Interferenz |
Die durch miRNA und siRNA programmierten RISC steuern unterschiedliche Ziele in der Zelle an. Die aus doppelsträngiger RNA gebildete siRNA wird bei Säugetieren einschließlich des Menschen offenbar nicht endogen gebildet. Eine ihrer grundlegenden Funktionen betrifft die Abwehr von Viren. Denn wenn virale doppelsträngige RNA zu siRNA zerhackt wird, lässt sich damit die Expression viraler Proteine unterdrücken. Allerdings antworten Viren auch mit Gegenstrategien. Durch sog. genetisches Engineering lässt sich doppelsträngige RNA in Zellen einschleusen und mit Hilfe der dann gebildeten siRNA die Überexpression bestimmter Gene unterdrücken. Hierdurch eröffnen sich unter Umständen zukünftige Therapieoptionen bei verschiedenen Krebserkrankungen. Andererseits haben etliche große Pharmafirmen nach Fehlschlägen bei siRNA-basierten Therapieansätzen diesbezügliche Projekte zumindest auf Eis gelegt.
Forschung und Industrie konzentrieren sich heute im Wesentlichen auf die miRNA. Diese hat eine erhebliche Bedeutung bei Tumorerkrankungen.
Über miRNA wird die Gen-Expression reguliert, so dass sie bei Wachstums- und Differenzierungsprozessen eines Organismus Schlüsselfunktionen
innehat. Etwa die Hälfte der miRNA-Gene ist in tumorassoziierten Regionen des Genoms oder in Fragile Sites lokalisiert. miRNA-Signaturen
von Krebsgeweben lassen sich analog zu mRNA-Signaturen mithilfe von miRNA-Mikroassays erhalten. Ihre Aussagekraft ist für verschiedene
Gewebe der von mRNA-Profilen überlegen. Als Diagnoseinstrument haben sie ihre Fähigkeit bei schlecht differenzierten Tumoren ungewisser
Herkunft unter Beweis gestellt. In einigen Fällen war es möglich, den Primärtumor anhand des miRNA-Profils zu identifizieren.
-
Das Spektrum der Behandlungsmöglichkeiten bei Prostatakrebs umfasst im Wesentlichen die engmaschige Überwachung (active surveillance)
die Strahlentherapie, die radikale Prostatektomie und die Androgendeprivationstherapie (ADT). Chemotherapien sind erst bei
kastrationsresistentem Prostatakrebs indiziert. Bei lokalisierter Krankheit in einem frühen Stadium erfolgt die radikale Prostatektomie
in kurativer Absicht. Andererseits ist Prostatakrebs oft relativ indolent, so dass die Überlegungen insbesondere bei Männern im
fortgeschrittenen Alter dahin gehen, dass eine Progression der Krankheit innerhalb der Lebenserwartung des Patienten eher
unwahrscheinlich ist. Um in solchen Fällen eine Überbehandlung zu vermeiden, bei der Nebenwirkungen die Lebensqualität in nicht
unerheblichem Maße einschränken können, lässt sich die Therapie unter Umständen unter engmaschiger Überwachung aufschieben oder
gar überflüssig machen.
Eine Reihe von Untersuchern hat bereits miRNA-Vergleiche in gesundem und malignem Prostatagewebe anhand von Mikroarray-Analysen
vorgenommen. Allerdings sind die Ergebnisse bislang eher ernüchternd. Verschiedene Autoren sind sich bei zahlreichen miRNA uneinig,
ob sie im Prostatakrebsgewebe herauf oder herunterreguliert sind (Übersicht in [1]). Hierfür kommen in erster Linie technische Ursachen
in Frage. Das reicht von der Selektion der Patientenpopulation mit unterschiedlichen Tumorstadien und Differenzierungsgraden wie auch
Behandlungseinflüssen über die Präparation und Behandlung des Ausgangsmaterials bis hin zur Verwendung von Gesamt-RNA oder angereicherter
kleiner RNA. Alles in allem sind es noch etliche weitere Details, die beachtet und standardisiert werden müssen, um die Vergleichbarkeit
von Mikroarray-
In einer jüngeren Analyse von Virologen an der Universität des Saarlands in Homburg/Saar wurden miRNA-Profile von Prostatakarzinomen
mittels deep sequencing erhalten. Das Team identifizierte 33 miRNA, die entweder um das 1,5-fache herauf- oder herunterreguliert
waren. Die Deregulierung selektionierter miRNA wurde durch Northern-
In Prostatakrebsproben waren miR-375 und miR-141 vermehrt exprimiert und ihre Freisetzung ins Blut stieg mit fortgeschrittenem
Krankheitsstadium an [3].
In einer kleinen Fallzahl wurden Korrelationen zwischen miRNA und kliniko-pathologischen Merkmalen bei Prostatakrebs ermittelt: miR-16
und miR-195 wie auch miR-26a waren signifikant mit positiven Schnitträndern assoziiert und miR-195 sowie miR-let7i korrelierten mit dem
Gleason Score [4].
-
Es gibt Indizien, dass miR-15a und miR-16 im Prostatakrebszellen als Tumorsuppressorgene wirksam sind [5].
Sie supprimieren die die Expression des antiapoptotischen Proteins BCL2, von CCND1 (kodiert für Zyklin D1) und von WNT3A,
die Überleben, Proliferation und Invasion von Prostatakrebs fördern. In den Zellen von fortgeschrittenen Prostatakarzinomen
waren die Spiegel an miR-15a und miR-16 signifikant erniedrigt und die Expression von BCL2, CCND1 und WNT3A deutlich erhöht.
In Xenotransplantaten bei Mäusen wurden nach Rekonstitution der Expression von miR-15a und miR-16 ein Wachstumsstop, Apoptose
und eine deutliche Regression des Tumors beobachtet.
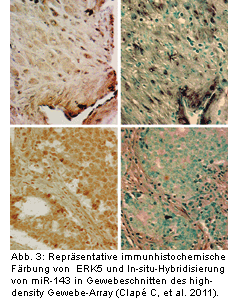
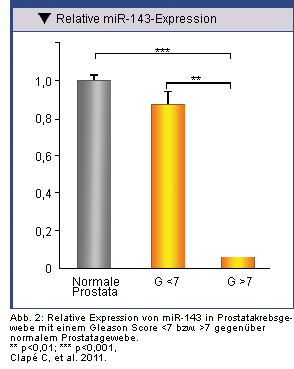
Als potenzielles Ziel für die Prostatakrebstherapie gilt auch miR-143. Seine Konzentration in Prostatakrebszellen ist umso geringer, je fortgeschrittener das Krankheitsstadium ist (Abb. 2). Nach Einbringen von miR-143 in Prostatakrebszellen durch Elektroporation in vivo bei Mäusen kam es zum Stillstand der Zellproliferation und des Tumorwachstums. Mithilfe von Bioinformatics-Analysen wurde ERK5 als ein potenzielles Ziel von miR-143 identifiziert. ERK5 fördert das Zellwachstum und die Zellproliferation als Reaktion auf Zellwachstumssignale und die Aktivierung von Tyrosinkinase. Es zeigte sich, dass ERK5 in Prostatakrebsgewebe verglichen mit normalem Prostatagewebe deutlich vermehrt exprimiert wurde (Abb. 3) [7].
Durch miRNA, die über die lange 3-untranslatierte Region (3UTR) des Androgenrezeptor (AR)-Gens dessen Expression regulieren, lassen
sich unter Umständen therapeutische Strategien entwickeln, die AR-Funktion und damit Androgen-abhängiges Wachstum zu inhibieren. Bei
der Analyse klinischer Prostatakarzinome ergab sich eine negative Korrelation insbesondere zwischen miR-34a wie auch miR-34c und den
AR-Spiegeln [8].
Literatur:
[1] Coppola V, De Maria R, Bonci D, et al. 2010. MicroRNAs and prostate cancer. Endocrine Related Cancer 17:F1-F17.
[2] Szczyrba J, Löprich E, Jung WS, et al. 2010. The microRNA profile of prostate carcinoma obtained by deep sequencing. Mol Cancer Res 8:529-538.
[3] Brase JC, Johannes M, Schlomm T, et al. 2011. Circulationg miRNAs are correlated with tumor progression in prostate cancer. Int J Cancer 128:608-616.
[4] Mahn R, Heukamp LC, Rogenhofer S, et al. 2011. Circulating microRNAs (miRNAs) in serum of patients with prostate cancer. Urology 77:1265.e9-e16.
[5] Bonci D, Coppola V, Mesumeci M, Addario A, 2008. The miR-15amiR-16-1 cluster controlls prostate cancer by targeting multiple oncogenic activities. Nat Med 14:1271-1277.
[6] Liu C, Kelnar K, Liu B, et al. 2011. The microRNA miR-34a inhibits prostatecancer stem cells and metastasis by directly repressing CD44. Nat Med 17:211-215.
[7] Clapé C, Fritz V, Henriquet C, et al. 2011. miR-143 interferes with ERK5 signalling, and abrogates prostate cancer progression in mice. PLoS ONE 4:e7542.
[8] Östling P, Leivonen SK, Aakula A , et al. 2011. Systematic analysis of microRNAs targeting the androgen receptor in prostate cancer cells. Cancer Res 71:1956-1967.
© 2003-2026 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz
