
Talazoparib-Monotherapie bei mCRPC-Patienten mit Mutationen in DNA-Reparaturgenen: TALAPRO-1
Poly(ADP-Ribose)-Polymerase (PARP)-Inhibitoren haben Antitumoraktivität gegen metastasierten kastrationsresistenten Prostatakrebs (mCRPC) mit DNA-Schadensantwort (DDR)-Mutationen, die bei der homologen Rekombinationsreparatur (HRR) eine direkte oder indirekte Rolle spielen. In der aktuellen Studie wurde der PARP-Inhibitor Talazoparib bei mCRPC mit DDR-Mutationen bewertet.
In der Phase-2-Open-label-Studie erhielten Patienten mit progredientem adenokarzinomatösem mCRPC orales Talazoparib (1 oder 0,75 mg pro Tag). Eignungskriterien waren messbare Weichteilmetastasen (per RECIST 1.1), ein ECOG-PS von 02, DDR-Mutationen (z.B. ATM, ATR, BRCA1, BRCA2, CHEK2, FANCA, MLH1, MRE11A, NBN, PALB2, RAD51C), der Erhalt 12 taxanbasierter Chemotherapien und Progression mit ≥1 neuen Hormontherapie. Primärer Endpunkt war die bestätigte objektive Ansprechrate (ORR, bestes gesamtes Weichteilansprechen per RECIST 1.1) durch unabhängigen, verblindeten zentralen Review.
Von 128 rekrutierten Männern verblieben 104 Patienten in der Antitumoraktivitätspopulation (AAP). Das mediane Follow-up betrug 16,4 Monate.
In der AAP hatten vier Patienten nur eine BRCA1-Alteration, 52 nur eine BRCA2-Alteration, 15 nur eine ATM-Alteration,
vier nur eine PALB2-Alteration und 22 hatten andere HRR-Mutationen.
In der AAP betrug die ORR-Rate 29,8% (31/104 Patienten). Nach hierarchischer Aufteilung der HRR-Mutationen betraf das 26 von 57 Patienten
mit BRCA2-Mutationen, zwei von vier mit BRCA1-Mutationen, einem von vier mit PALB2-Mutationen und zwei von 17 mit ATM-Mutationen.
In Post-hoc-Analysen wurde bei 26 von 68 Patienten ohne viszerale Metastasen und bei fünf von 36 Patienten mit viszeralen Metastasen
objektives Ansprechen festgestellt.
Bei den 36 verbliebenen Patienten betraf das objektive Ansprechen einen von 20 Patienten mit Lebermetastasen und vier
von 16 ohne Lebermetastasen.
Bei den meisten Patienten in der AAP mit Bewertungen sowohl zu Baseline als auch post-baseline wurde eine Verminderung der Tumorlast (67/84),
des PSA-Spiegels (69/96) und der zirkulierenden Tumorzellen (37/45) registriert. Die höchste Rate fand sich bei Patienten
mit BRCA1- oder BRCA2-Mutationen.
Bei den meisten auswertbaren Patienten mit PALB2- oder ATM-Mutationen waren auch die Tumorlast, der PSA-Spiegel
und die zirkulierenden Tumorzellen erniedrigt.
Eine Reduktion der Tumorlast und des PSA war von der DDR-HRR-Genalteration unabhängig. Allerdings wurde eine Abnahme der Tumorgröße
oder des PSA von 30% oder
darüber primär bei homozygoten Mutationen ermittelt.
|
|
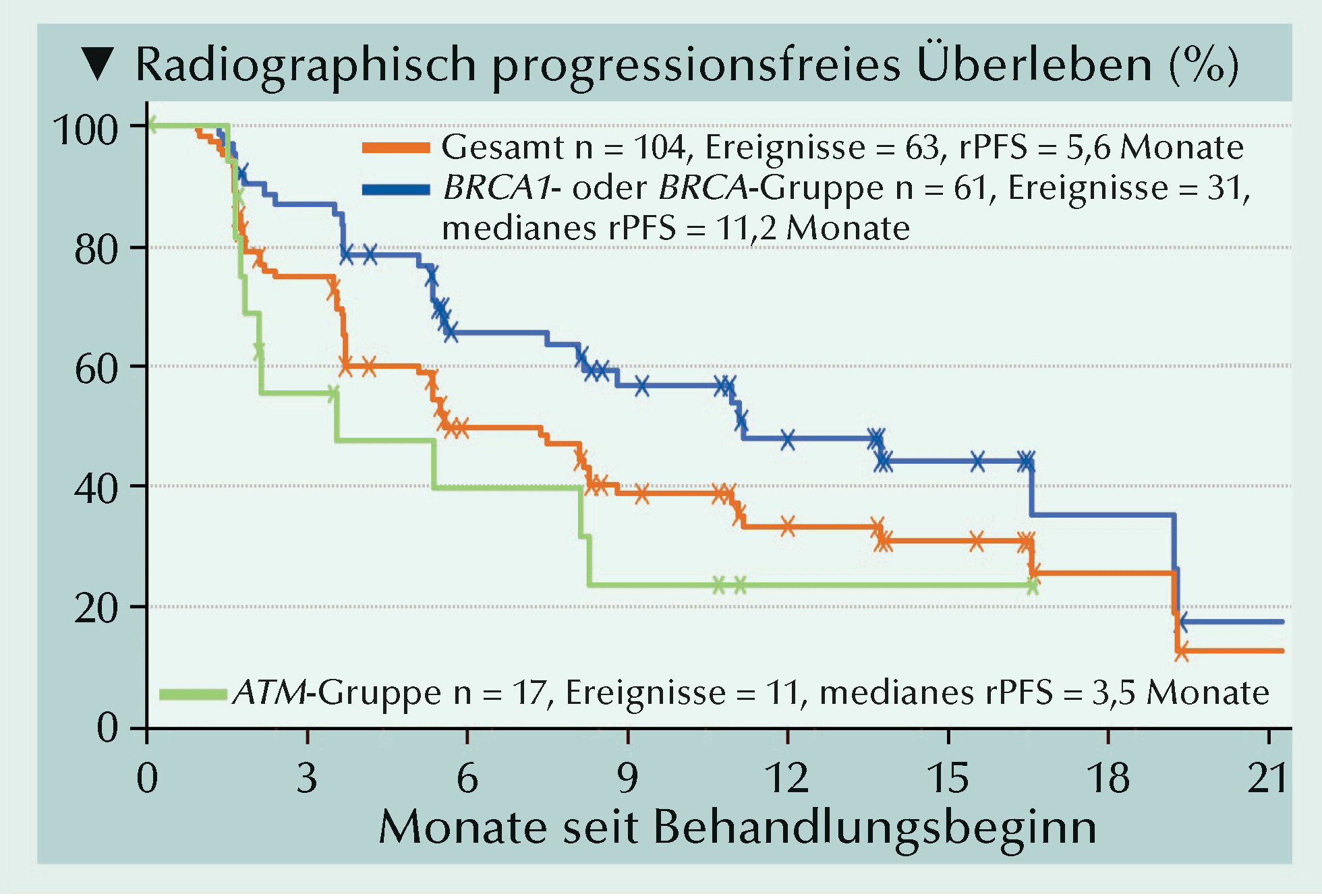
Abb.: Radiographisch progressionsfreies Überleben (rPFS) gesondert nach Gesamtpopulation,
BRCA1-/BRCA2-Mutationen und ATM-Mutationen. HRR = homologe Rekombinationsreparatur. |
Die häufigsten behandlungsverursachten unerwünschten Ereignisse der Grade 34 waren Anämie (39 von 127 Patienten), Thrombozytopenie (11) und Neutropenie (10). Schwerwiegende Fälle betrafen 43 Patienten, ohne dass es zu Todesfällen kam.
❏ Das vorteilhafte Nutzen-Risiko-Profil spricht für die Untersuchung von Talazoparib in größeren, randomisierten klinischen Studien auch bei Patienten mit Mutationen in anderen, für die DNA-Reparatur wichtigen Genen als den BRCA-Genen.
© 2003-2026 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz