
erektion — ejakulation — penis — hoden — endokrinologie — fertilität — genetische aspekte — aging male — varia

Oligozoospermie bzw. Azoospermie, hypergonadotroper Hypogonadismus und kleine, feste Hoden sind wesentliche
Charakteristika von Männern mit Klinefelter-Syndrom. Hierdurch ist die reproduktive Funktion der betroffenen
Männer äußerst stark beeinträchtigt. Erst seit der Entwicklung effektiver Methoden der assistierten Reproduktion
(ART) besteht für zahlreiche Männer mit Klinefelter-Syndrom die realistische Chance auf eine Vaterschaft.
-
Bei Männern mit Klinefelter-Syndrom sind neben den beiden Geschlechtschromosomen XY in allen oder einer größeren
Zahl der Körperzellen ein oder mehrere überzählige X-Chromosomen vorhanden. Hierbei ist der Karyotyp 47,XXY mit
etwa 80% am häufigsten vertreten (Abb. 1).Das überschüssige X-Chromosom stammt aus einer Fehlverteilung der
Geschlechtschromosomen während der ersten oder zweiten meiotischen Teilung. Aber auch noch während mitotischer
Teilungen in der frühen Zygote kann es zu einer solchen Fehlverteilung kommen. Hierbei entwickeln sich so
genannte Mosaike (Abb. 2).

|
Abb. 1:. |
-
Klinefelter-Patienten gelten allgemein als infertil. Dennoch gibt es sporadisch Berichte, wonach Männer mit
Klinefelter-Syndrom (auch Nicht-Mosaike) Väter gesunder Kinder geworden sind [1, 2]. Ermöglicht wird
das fast ausschließlich mit Hilfe der intrazytoplasmatischen Spermium-Injektion (ICSI), sofern sich bei dem
Mann durch testikuläre Spermien-Extraktion (TESE) Keimzellen gewinnen lassen.
Chromosomenanomalien kommen bei Klinefelter-Patienten (47,YYY und 46,XY/47,XXY) nicht häufiger vor als bei
anderen Infertilitätspatienten [3].
|
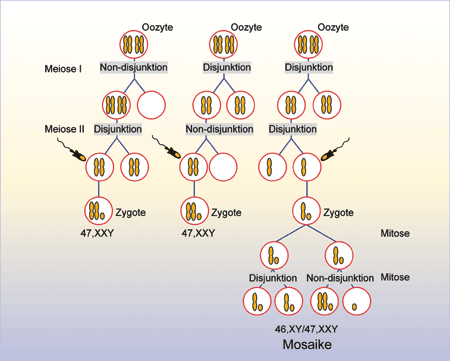
Abb. 2: Entstehung des 47,XXY-Karyotyps während der ersten oder zweiten meiotischen Teilung im Rahmen der Oogenese und von Mosaiken (46,xxY/47,XXY) während der ersten mitotischen Teilung der Zygote: Zellen mit einem XXY-Karyotyp sind das Resultat einer nicht stattgefundenen Separation der gepaarten Chromosomen (Non-disjunction) im Rahmen der Karyokinese (Kernteilung). Wie bei der Oogenese kann eine Non-disjunktion auch bei der Spermiogenese auftreten. |
-
Die Degeneration der Tubuli seminiferi bei 47,XXY-Männern beginnt bereits während der Fetalphase, setzt sich im
Kindesalter fort und beschleunigt sich während der Pubertät dramatisch [4].
Bei Untersuchungen von Hoden-biopsien in einer Studie mit 47,XXY-Jungen (n = 14) fanden Wikström et al. [5] in keinem Fall meiotische Keimzellen.
Keimzellen werden bei Männern mit Klinefelter-Syndrom entweder noch vor Einsetzen der Meiose als Spermatogonien B
oder unmittelbar zu Beginn der Meiose noch vor Erreichen des Leptotän-Stadiums eliminiert [6].
-
Bei Männern mit Klinefelter-Syndrom besteht eine eindeutige Indikation zur Testosteronsubstitution. Hiermit
sollte möglichst frühzeitig begonnen werden. Verschiedentlich wurde sogar angeregt, mit der Substitution bereits
im Adoleszentenalter zu beginnen. Doch lässt sich vor und während der Pubertät ein Testosteronmangel überhaupt
nachweisen?
Bei Säuglingen mit Klinefelter-Syndrom steigt der Testosteronspiegel wie bei Jungen mit einem normalen Chromosomensatz postnatal physiologischerweise an. Allerdings bleibt der Anstieg bei Neugeborenen mit Klinefelter-Syndrom tief im unteren Referenzbereich [7].
Ergebnisse aus Experimenten mit Rhesusaffen lassen darauf schließen, dass sich ein mangelnder postnataler Testosteronanstieg nachteilig auf das Erlangen der sexuellen Kompetenz im Erwachsenenalter auswirken könnte.
Bei Jungen mit Klinefelter-Syn-drom wurden ab dem 13. Lebensjahr erhöhte Spiegel an Follikel-stimulierendem Hormon (FSH) und Luteinisierungshormon (LH) gemessen, obwohl der Testosteronspiegel zu diesem Zeitpunkt im Normbereich lag. Zugleich wurde eine überhöhte Gonadotropin-Ausschüttung als Reaktion auf einen Stimulus mit Gonadotropin-Releasing-Hormon (GnRH) registriert [8].
Die Ergebnisse von Wikström et al. [8] haben während der frühen Pubertät keinen ausgeprägten Testosteronmangel
erkennen lassen, der die Einleitung einer Substitution zu diesem Zeitpunkt routinemäßig erforderlich machte. Allerdings
mahnen die Autoren klinische Studien an, in denen eine frühzeitige Testosteronsubstitution hinsichtlich möglicher
Benefits bei der neuronalen Entwicklung und im psychosozialen Bereich geprüft werden sollte.
-
Um die Chancen einer Vaterschaft für Männer mit Klinefelter-Syndrom zu erhöhen, wird in letzter Zeit diskutiert,
Hodengewebe möglichst frühzeitig vor einer Substitution mit Testosteron durch Kryopreservation zu sichern. Eine
solche Maßnahme erreichte in jedem Fall nur jene Minderheit, bei der das Klinefelter-Syndrom bereits vor der Pubertät
diagnostiziert wird [9].
Damani et al. [10] berichteten von einem 15-jährigen Klinefelter-Patienten, bei dem aus den Hoden drei Spermien enthaltende Gewebeproben entnommen und kryokonserviert worden sind.
Das Alter stellt einen begrenzenden Faktor für die Aussicht dar, bei Männern mit Klinefelter-Syndrom erfolgreich Spermien zu gewinnen. Eine TESE bei Klinefelter-Patienten sollte daher vor dem 35. Lebensjahr erfolgen [11].
Wikström et al. [5] fanden in den Hoden frühpubertärer 47,XXY-Jungen keine mitotischen Keimzellen und sind daher
der Meinung, dass die Frühpubertät kein Zeitfenster für die Sicherung von Hodengewebe sei, mit dem sich die spätere
Fertilitätschance erhöhen lässt.
Literatur:
[1] Tachdjian G, Frydman N, Morichon-Delvallez N, et al. 2003.
Reproductive genetic counselling in non-mosaic 47, XXY patients: implications for preimplantation or prenatal diagnosis:
case report and review. Hum Reprod 18:271-275.
[2] Denschlag D, Tempfer C, Kunze M, et al. 2004.
Assisted reproductive techniques in patients with Klinefelter syndrome: a critical review. Fertil Steril 82:775-779.
[3] Rives N, Joly G, Machy A, et al. 2000. Assessment of sex chromosome aneuploidy in sperm nuclei
from 47,XXY and 46XY/47XXY males: comparison with fertile and infertile males with normal karyotype. Mol Hum Reprod 6:107-112.
[4] Aksglaede L, Wikström AM, Raipert-De Meyts E, et al. 2006.
Natural history of seminiferous tubule degeneration in Klinefelter syndrome. Hum Reprod Update 12:39-48.
[5] Wikström AM, Raivio T, Hadziselimovic F, et al. 2004.
Klinefelter syndrome in adolescence: onset of puberty is associated with accelerated germ cell depletion.
J Clin Endo-crinol Metab 89:2263-2270.
[6] Wikström AM, Hoei-Hansen CE, Dunkel L, Raipert-De Meyts E. 2006.
Immunoexpression of androgen receptor and nine markers of maturation in the testes of adolescent boys with
Klinefelter syndrome: evidence for degeneration of germ cells at the onset of meiosis. J Clin Endocrinol Metab 92:714-719.
[7] Lahlou N, Fennoy I, Carel J-C, Roger M. 2004.
Inhibin B and Anti-Müllerian hormone, but not testosterone levels, are normal in infants with nonmosaic Klinefelter syndrome.
J Clin Endocrinol Metab 89:1864-1868.
[8] Wikström AM, Dunkel L, Wickman S, et al. 2006.
Are adolescent boys with Klinefelter syndrome androgen deficient? A longitudinal study of Finnish 47,XXY boys.
Pediatr Res 59:854-859.
[9] Bojesen A, Juul S, Gravholt CH. 2003.
Prenatal and postnatal prevalence of Klinefelter syndrome: a national registry study. J Clin Endocrinol Metab 88:622-626.
[10] Damani MN, Mittal R, Oates RD. 2001. Testicular tissue extraction in a young male with 47,XXY Klinefelter´s syndrome:
potential strategy for preservation of fertility. Fertil Steril 76:1954-1056.
[11] Okada H, Goda K, Yamamoto Y, et al. 2005. Age as a limiting factor for successful sperm retrieval in patients
with non-mosaic Klinefelter´s syndrome. Fertil Steril 84:1662-1664.
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz
