Muskelinvasives Urothelkarzinom der Harnblase: |
||||||||
 Empfohlener Behandlungsstandard bei muskelinvasivem Blasenkarzinom (MIBC) ist die radikale Zystektomie (RZ)
mit beidseitiger pelviner Lymphadenektomie. Bei Patienten, die für Cisplatin in Frage kommen, sollte dem
eine neoadjuvante Chemotherapie vorausgehen. Mit einer Reihe von Begründungen hat sich das
in der Behandlung des MIBC jedoch nicht grundsätzlich durchsetzen können, d. h. nur etwa 20% der dafür geeigneten Patienten
erhalten eine neoadjuvante Chemotherapie. In jüngerer Zeit hat sich das therapeutische Potenzial für Patienten mit
Urothelkarzinom durch die Einführung der Immun-Checkpoint-Inhibitoren deutlich erweitert. Damit ließe sich die
Kurzbehandlung mit einer Immuntherapie vor der RZ in das neoadjuvante Behandlungskonzept bei nicht
metastasiertem MIBC integrieren.
Empfohlener Behandlungsstandard bei muskelinvasivem Blasenkarzinom (MIBC) ist die radikale Zystektomie (RZ)
mit beidseitiger pelviner Lymphadenektomie. Bei Patienten, die für Cisplatin in Frage kommen, sollte dem
eine neoadjuvante Chemotherapie vorausgehen. Mit einer Reihe von Begründungen hat sich das
in der Behandlung des MIBC jedoch nicht grundsätzlich durchsetzen können, d. h. nur etwa 20% der dafür geeigneten Patienten
erhalten eine neoadjuvante Chemotherapie. In jüngerer Zeit hat sich das therapeutische Potenzial für Patienten mit
Urothelkarzinom durch die Einführung der Immun-Checkpoint-Inhibitoren deutlich erweitert. Damit ließe sich die
Kurzbehandlung mit einer Immuntherapie vor der RZ in das neoadjuvante Behandlungskonzept bei nicht
metastasiertem MIBC integrieren.
 Die Wirksamkeit von Pembrolizumab als neoadjuvante Immuntherapie vor der RZ
bei MIBC sollte ermittelt werden.
Die Wirksamkeit von Pembrolizumab als neoadjuvante Immuntherapie vor der RZ
bei MIBC sollte ermittelt werden.
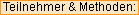 Die Patienten der einarmigen Open-Label-Phase-II-Studie PURE-01 hatten überwiegend ein urotheliales
Karzinom (cT≤3bN0). Sie erhielten vor der RZ drei Zyklen Pembrolizumab 200 mg Q3W.
Als primärer Endpunkt in der Intention-to-treat-Population war pathologisch komplettes Ansprechen (pT0)
gewählt worden.
Biomarker-Analysen umfassten die programmed death-ligand 1 (PD-L1)-Expression anhand des mit dem Dako 22C3 pharmDx-Assay
immunhistochemisch ermittelten kombinierten positiven Score (CPS), die Genom-Sequenzierung und die Immungen-Expression.
Die Patienten der einarmigen Open-Label-Phase-II-Studie PURE-01 hatten überwiegend ein urotheliales
Karzinom (cT≤3bN0). Sie erhielten vor der RZ drei Zyklen Pembrolizumab 200 mg Q3W.
Als primärer Endpunkt in der Intention-to-treat-Population war pathologisch komplettes Ansprechen (pT0)
gewählt worden.
Biomarker-Analysen umfassten die programmed death-ligand 1 (PD-L1)-Expression anhand des mit dem Dako 22C3 pharmDx-Assay
immunhistochemisch ermittelten kombinierten positiven Score (CPS), die Genom-Sequenzierung und die Immungen-Expression.
 Von Februar 2017 bis März 2018 wurden 50 Patienten an zwei Mailänder Zentren in die Studie aufgenommen.
Von Februar 2017 bis März 2018 wurden 50 Patienten an zwei Mailänder Zentren in die Studie aufgenommen.Patientencharakteristika: Von ihnen waren 46 (92%) für eine Cisplatin-Chemotherapie geeignet. Mehrheitlich(54%) waren es Tumore im Stadium cT3. Zwei nicht für Cisplatin in Frage kommende Patienten wurden aufgenommen, obwohl bei ihnen Indizien für Nodalpositivität vorlagen.
Die mediane Behandlungsdauer mit Pembrolizumab betrug 63 Tage (57–70 Tage).
Ein Patient erlitt einen Grad-3-Transaminaseanstig und beendete die Behandlung mit Pembrolizumab.
Alle Patienten unterzogen sich der RZ. 23 Behandlungen wurden als fehlgeschlagen gewertet. Bei zehn Patienten lag eine pathologische Lymphknotenbeteiligung vor. Bei 5 Patienten wurde nach Ermessen des Arztes eine sequentielle Chemotherapie mit Methotrexat, Vinblastin, Doxorubicin und Cisplatin (MVAC) verabreicht (kein radiologisches Ansprechen [n=4] und Absetzen von Pembrolizumab aufgrund Grad-3-Transaminitis [n=1]). Zwei dieser Patienten wurden mit der Chemotherapie auf pTis heruntergestuft.
Zum Zeitpunkt des Datenabschlusses (10. Juni 2018) betrug das mediane Follow-up 6,2 Monate.
Insgesamt 26 Patienten (52%) hatten deletäre DNA-Schadensregulierungs- (DDR; DNA damage response and repair) oder RB1-Genmutationen (Abb.). In diesen Fällen lag die mediane Tumormutationslast höher als in Fällen ohne solche Mutationen (median 13,2 Mut/Mb vs. median 9,7 Mut/Mb; p=0,008). Bei der Behandlung des fortgeschrittenen Urothelkarzinoms mit Immun-Checkpoint-Inhibitoren waren bereits zuvor Alterationen in DDR-Genen mit klinischem Benefit in Zusammenhang gebracht worden. Nur für PBRM1 wurde die Assoziation eines Einzelgens mit pT0-Ansprechen nachgewiesen (Abb.).
Bei pT0-Respondern und pT0-Nicht-Respondern differierte die Expression mehrerer Gene in den Tumoren
vor der Therapie signifikant.
Necchi A, Anichini A, Raggi D, et al. 2018. Pembrolizumab as neoadjuvant therapy before radical cystectomy in patients with muscle-invasive urothelial bladder carcinoma (PURE-01): An open-label, single-arm, phase II study. J Clin Oncol DOI: 10.1200/JCO.18.01148. |
||||||||
| ||||||||