Fortgeschrittener Urothelkrebs: |
 Die initialen Ergebnisse der Phase-2-Studie KEYNOTE-052 waren Grundlage für die Zulassung von Pembrolizumab
zur Behandlung nicht Cisplatin-geeigneter Patienten mit fortgeschrittenem Urothelkarzinom (UC).
Auf dem ASCO 2019 wurden aktualisierte Ergebnisse vorgestellt, die ein Follow-up von mehr als 2 Jahren
seit der Rekrutierung des letzten Patienten umfassen.
Die initialen Ergebnisse der Phase-2-Studie KEYNOTE-052 waren Grundlage für die Zulassung von Pembrolizumab
zur Behandlung nicht Cisplatin-geeigneter Patienten mit fortgeschrittenem Urothelkarzinom (UC).
Auf dem ASCO 2019 wurden aktualisierte Ergebnisse vorgestellt, die ein Follow-up von mehr als 2 Jahren
seit der Rekrutierung des letzten Patienten umfassen.
 Wirksamkeit und Verträglichkeit einer Erstlinien-Monotherapie mit Pembrolizumab sollten bei Patienten mit lokal fortgeschrittenem
oder metastasiertem UC, die nicht für eine Cisplatin-Chemotherapie in Frage kommen, geprüft und über einen Zeitraum
von mindestens zwei Jahren nach Aufnahme des letzten Teilnehmers nachverfolgt werden.
Auf dem ASCO 2019 wurden Langzeit-Ergebnisse von KEYNOTE-052 vorgestellt.
Wirksamkeit und Verträglichkeit einer Erstlinien-Monotherapie mit Pembrolizumab sollten bei Patienten mit lokal fortgeschrittenem
oder metastasiertem UC, die nicht für eine Cisplatin-Chemotherapie in Frage kommen, geprüft und über einen Zeitraum
von mindestens zwei Jahren nach Aufnahme des letzten Teilnehmers nachverfolgt werden.
Auf dem ASCO 2019 wurden Langzeit-Ergebnisse von KEYNOTE-052 vorgestellt.
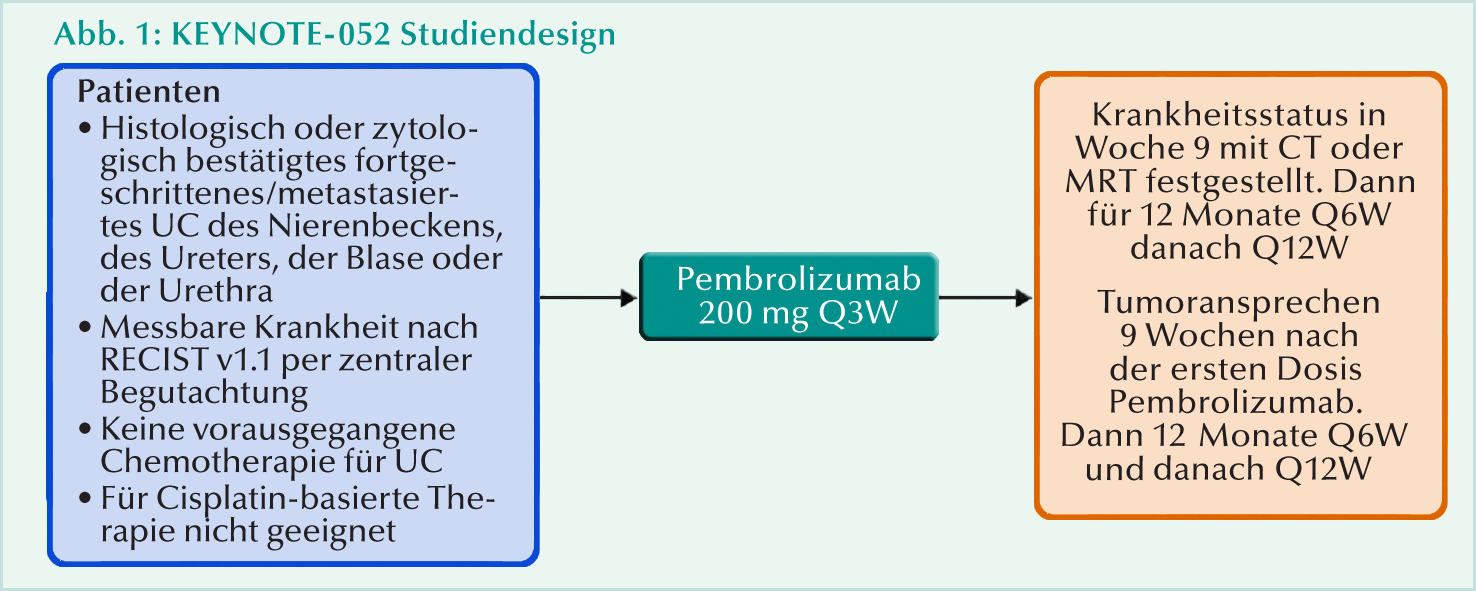
 Das Studiendesign ist aus Abb. 1 ersichtlich. Die Behandlung wurde bis
Das Studiendesign ist aus Abb. 1 ersichtlich. Die Behandlung wurde bis
Sekundäre Endpunkte waren:
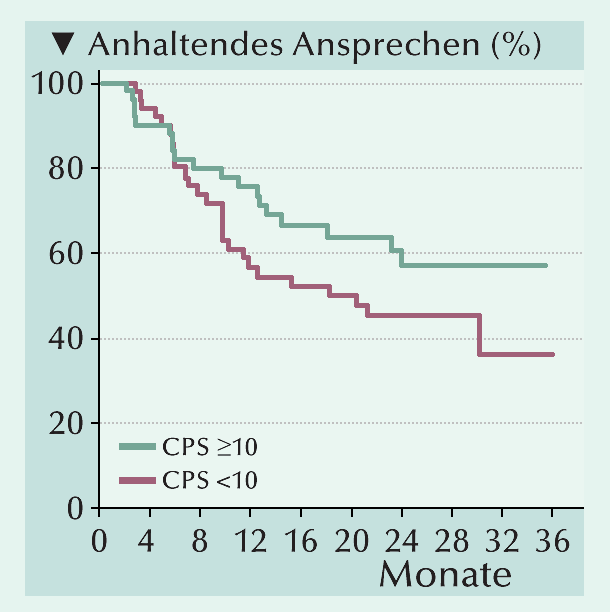
 Objektive Ansprechrate (ORR): In der gesamten Kohorte (n=370) betrug die ORR 28,6% (8,9% Komplettansprechen und 19,7% partielles Ansprechen). Stabile Krankheit wurde in 18,1% der Fälle und Krankheitsprogress in 42,4% der Fälle registriert. Bei den Patienten mit einem CPS ≥10 (n=110) betrug die ORR 47,3% (20,0% Komplettansprechen und 27,3% partielles Ansprechen). Stabile Krankheit resultierte in 20,0% der Fälle und Krankheitsprogress in 27,3%. Eine ORR erreichten 25/51 (49%) Patienten mit Metastasen nur in den Lymphknoten und 79/315 (25,1%) der Patienten mit viszeralen Metastasen. Dauer des Ansprechens (DOR): Als mediane DOR wurden in der Gesamtpopulation 30,1 Monate (95% KI 18,8–nicht erreicht) ermittelt. Bei Patienten mit CPS ≥10 war die mediane DOR noch nicht erreicht. Bei den Patienten mit CPS <10 betrug sie 18,2 Monate (Abb. 2). Progressionsfreies Überleben (PFS): Das mediane PFS der Gesamtkohorte betrug 2,2 Monate. Ein 6- und 12-monatiges PFS erreichten 33,4% bzw. 22,0% der Patienten Gesamtüberleben (OS): Das mediane OS von 13,3 Monaten in der Gesamtpopulation verteilte sich auf 18,5 Monate für die Patienten mit einem CPS ≥10 und auf 9,7 Monate bei einem CPS <10. Von ihnen überlebten 47,0% bzw. 24,0% die 24-Monatsmarke.
Sicherheit und Verträglichkeit: Behandlungsbezogene Nebenwirkungen kamen bei 67% der Patienten vor.
Am häufigsten waren Fatigue und Pruritus (jeweils 18%). In 21% der Fälle waren sie vom Grad ≥3; davon
ein Todesfall (Myositis).
O´Donnell PH, Balar AV, Vuky J, et al. 2019. KEYNOTE-052 phase 2 study evaluating first-line pembrolizumab in cisplatin-ineligible advanced urothelial cancer. Updated response and survival results. J Clin Oncol 37(15_suppl):4546-4546. |
|||
| ||||