Therapie nach ADT-basierter Kombinationstherapie patientengerecht planen
Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) sollten im Therapieverlauf alle lebensverlängernden Therapieoptionen erhalten. Therapieentscheidung und Therapiesequenz orientieren sich an verschiedenen Kriterien, unter anderem auch an der Vorbehandlung im hormonnaiven Stadium der metastasierten Erkrankung. Hier steht mit der Kombinationstherapie aus Androgendeprivation (ADT) plus Chemotherapie (Docetaxel) bzw. gegen den Androgenrezeptor gerichteten Substanzen (ARTA) ein neuer Standard zur Verfügung. Das beeinflusst auch die Behandlung im mCRPC-Stadium.
Für die beiden Taxane Docetaxel (Taxotere®) und Cabazitaxel (Jevtana®) ist in
randomisierten Phase-III-Studien bei Patienten mit mCRPC eine lebensverlängernde
Wirkung belegt [1,2]. Bei der Planung der Therapiesequenz sollte daher berücksichtigt
werden, dass die Chemotherapie keinem Patienten vorenthalten werden sollte, zum
Beispiel weil diese erst zu spät eingesetzt wird und der Patient dann eventuell
nicht mehr Chemotherapie-fit ist, betonte PD Dr. med. Maria De Santis, Charité Berlin.
Zudem sprechen nicht alle Patienten auf eine endokrine Therapie an. Ein Hinweis auf
eine primäre endokrine Resistenz sei ein nur kurzes Ansprechen auf die ADT (<12 Monate)
im hormonnaiven Stadium [3,4]. Darüber hinaus sieht De Santis eine Chemotherapie-Indikation
im mCRPC-Stadium bei symptomatischen Patienten, bei tumorbedingt schlechtem Allgemeinzustand
sowie bei Nachweis von Lebermetastasen. Unabhängig davon käme eine Chemotherapie bei kurzer
PSA-Verdopplungszeit (<55 Tage), hohem Gleason Score (8 bis 10) und einem hohen LDH bzw.
ALP in Betracht [3,4].
Kreuzresistenz der ARTAs beachten
Im hormonnaiven Stadium hat sich mit der ADT-basierten Kombinationstherapie ADT/Docetaxel
bzw. ADT/Abirateron ein neuer Standard etabliert [5,6,7,8]. Für die Therapieentscheidung
im mCRPC-Stadium müsste in Anbetracht des Mangels entsprechender Studien extrapoliert
werden: Studiendaten beim mCRPC weisen auf Kreuzresistenzen zwischen den ARTAs hin [9],
weshalb das Therapieansprechen auf die zweite ARTA gering und nur von kurzer Dauer sei,
so De Santis. Eine Sequenz aus zwei ARTAs mache daher keinen Sinn. Für mit ADT/ARTA
behandelte Patienten sei daher die Weiterbehandlung mit einer ARTA im mCRPC-Stadium
nicht zu empfehlen, stellte De Santis fest.
Vorteile der Sequenz Docetaxel Cabazitaxel nutzen
Keine Kreuzresistenz bestehe zwischen Docetaxel und Cabazitaxel. Im Gegenteil:
Cabazitaxel ist eine wirksame Therapieoption nach Docetaxel-Versagen [2], wurde
speziell für die Situation nach Docetaxel-Versagen entwickelt und ist für diese
Indikation zugelassen [10]. Zudem zeigen retrospektive Studiendaten zur Sequenztherapie
beim mCRPC, dass Patienten, die nach Docetaxel zunächst mit Cabazitaxel gefolgt von
einer ARTA behandelt werden, in der dritten Linie länger überleben, als jene, die
nach Docetaxel eine ARTA gefolgt von Cabazitaxel erhalten [11]. Für Patienten, die
mit ADT/Docetaxel im hormonnaiven Stadium vorbehandelt wurden, sei daher bei
Chemotherapie-Indikation die Weiterbehandlung mit Cabazitaxel im mCRPC-Stadium
der Docetaxel-Reinduktion vorzuziehen, betonte De Santis. Französische Studiendaten
zeigten hier einen deutlichen Wirksamkeitsverlust unter Docetaxel-Reinduktion [12].
Besteht keine Chemotherapie-Indikation nach ADT/Docetaxel, empfiehlt De Santis
im mCRPC-Stadium Cabazitaxel als Zweitlinien-Option nach ARTA. Aufgrund der
Kreuzresistenz zwischen den ARTAs sei der Einsatz einer zweiten ARTA keine Option,
erinnerte De Santis.
Positiver Einfluss der Chemotherapie auf die Lebensqualität
Die Chemotherapie erhält bzw. verbessert zudem die Lebensqualität von Patienten
mit metastasiertem Prostatakarzinom (mPC), ergänzte Dr. med. Stefan Machtens, Bergisch Gladbach.
Prospektive Daten aus dem klinischen Alltag bestätigen dies: In der CAPRISTANA-Studie [13]
beispielsweise, eine nicht-interventionelle Kohortenbeobachtungsstudie, konnten
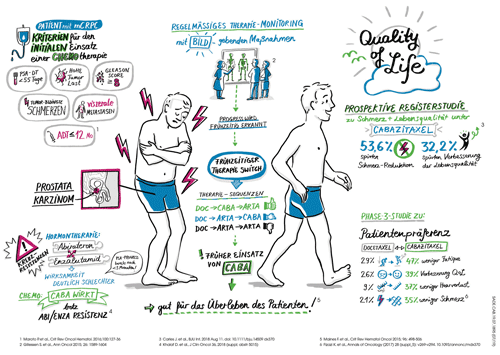
Schmerzen unter Cabazitaxel bei 53,6 Prozent der Patienten gelindert werden und bei
32,2 Prozent verbesserte sich die gesundheitsbezogene Lebensqualität (FACT-P-Score).
Laut QoLiTime-Studie [14], eine nicht-interventionelle Beobachtungsstudie, hatten
Patienten mit einem PSA-Abfall >50 Prozent eine besonders deutliche
Schmerzreduktion (p=0,01). In der prospektiven Registerstudie SEQOND [15]
hatten Patienten mit mCRPC unter Cabazitaxel eine vergleichbare Lebensqualität wie jene,
die Abirateron erhalten hatten. Die randomisierte Phase-III-Studie CABADOC [16]
unterstreiche die bessere Verträglichkeit von Cabazitaxel versus Docetaxel,
so Machtens: Von 195 Patienten mit mCRPC präferierten 43 Prozent Cabazitaxel und
27 Prozent Docetaxel; die restlichen Patienten hatten keine Präferenz. Die Patienten
gaben unter Cabazitaxel insbesondere seltener Fatigue, Schmerzen und Haarverlust sowie
insgesamt eine bessere Lebensqualität an.
Die empfundene Lebensqualität korreliere primär mit dem Behandlungserfolg und
nicht mit den Nebenwirkungen, resümierte Machtens. Besteht eine Chemotherapie-Indikation,
sei es wichtig, die Chemotherapie frühzeitig einzusetzen, die Akzeptanz des Patienten
gegenüber dieser zu stärken und über ihre Chancen als lebensverlängernde
Therapie aufzuklären.
|
Referenzen:
[1] Tannock IF, et al., NEJM 2004, 351:1502-12.
[2] de Bono JS, et al., Lancet 2010, 376:1147- 54.
[3] Angelergues A, et al. Clin. Genitourin. Cancer 2018 Aug;16(4):e777-e784
[4] Maroto P, et al., Crit Rev Oncol Hematol 2016, 100:127-36.
[5] Sweeney C, et al., NEJM 2015, 373:737-46.
[6] James ND, et al., Lancet 2016, 387:1163-70.
[7] S3-Leitlinie zur Früherkennung, Diagnose und Therapie der verschiedenen
Stadien des Prostatakarzinoms. Version 5.0 April 2018. AWMF-Registernummer: 043/022OL.
[8] Fizazi K, et al., NEJM 2017, 377:352-60.
[9] Attard G, et al., JCO 2018, 36:2639-46.
[10] Fachinformation Jevtana®. Aktueller Stand.
[11] Maines F, et al., Crit Rev Oncol Hematol 2015, 96:498-506.
[12] Lavaud P, et al., Eur Urol 2018, 73(5):696-703.
[13] Carles J, et al., BJU int 2019, 123:456-464.
[14] Hofheinz RD, et al., BJU int 2017, 119:731-740.
[15] Stenner F, et al., Clin Genitourin Cancer 2017 Aug 24. Pii:S1558-7673(17)30244-6.
[16] Baciarello G, et al., JCO 2019, 37:(supplabstract: 5017).
Quelle: Fachpresse-Workshop 10. Expertise Prostata am 3. Juli 2019 in Berlin. Veranstalter: Sanofi Genzyme
| 29. Juli 2019 |
Warning: include(../cols3/aa_meldungen.php): failed to open stream: No such file or directory in /var/www/web383/html/uros/meldungen/aa_2019_juli_sanofi_expertise_prostata.php on line 185
Warning: include(../cols3/aa_meldungen.php): failed to open stream: No such file or directory in /var/www/web383/html/uros/meldungen/aa_2019_juli_sanofi_expertise_prostata.php on line 185
Warning: include(): Failed opening '../cols3/aa_meldungen.php' for inclusion (include_path='.:/opt/php/5.4.45/share/pear:/usr/share/pear') in /var/www/web383/html/uros/meldungen/aa_2019_juli_sanofi_expertise_prostata.php on line 185
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz