|

|
November 2004 |
|
|
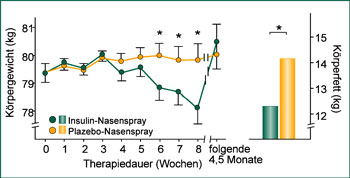
Gewichtsreduktion mit Insulin-Nasenspray |
|||
Insulin gehört zu den Botenstoffen, die an das Gehirn melden, wieviel Energie in Form von gespeichertem Fett vorrätig ist. Der Spiegel des Insulins im zirkulierenden Blut – wie auch der des Leptins – steigt und fällt mit zunehmendem bzw. abnehmendem Körperfettgehalt. Bei einer Nahrungskarenz wird Insulin vermindert ausgeschüttet. Der fallende Insulinspiegel wird vom Gehirn registriert und verarbeitet. Aus dem Hypothalamus werden daraufhin orexigene Signale (orexis = Appetit, Hunger) ausgesandt, die zur Nahrungsaufnahme animieren. Umgekehrt würde das Hungergefühl unterdrückt, wenn vermehrt Insulin ins Gehirn gelangt. Dies läßt sich durch Aufnahme von Insulin über die Nasenschleimhaut erreichen (Hallschmid M, et al. 2004): Männer nehmen ab, Frauen hingegen zu
Die gleiche Behandlung führte bei Frauen (n = 8) zu einer signifikanten Gewichtszunahme von 1,04 kg, die durch eine extrazelluläre Wassereinlagerung hervorgerufen wurde. Insulin gelangt über die Nasenschleimhaut direkt ins Gehirn Bei intranasaler Applikation gelangt Insulin in die zerebrospinale Flüssigkeit,
ohne daß sich die Insulinkonzentration in der Zirkulation erhöht. Von der Nasenschleimhaut
können Stoffe entlang der Riechnerven via Lamina cribrosa des Siebbeins
unmittelbar ins Gehirn gelangen.
Insulin wirkt im Gehirn als anorexigenes Signal
Insulin wie auch Leptin regulieren das Körpergewicht von Zentren im Hypothalamus aus.
Als anorexigenes Signal fungiert jeweils das Melanokortin. Dieser Mechanismus führt bei
beiden Geschlechtern zu einer reduzierten Nahrungsaufnahme. Offenbar werden
die Insulin- und Leptin-Signale im Gehirn bei Männern und Frauen unterschiedlich
verarbeitet.
|
|||
|
Hallschmid M, Benedict C, Schultes B, et al.
2004. Intranasal Insulin reduces body fat in men but not in women.
Diabetes 53:3024-3029. |
|||
|
|||