|

|
Januar 2004 |
|
| Welche Rolle spielen Sexualsteroide beim Erhalt der kardiovaskulären Gesundheit? |
|||
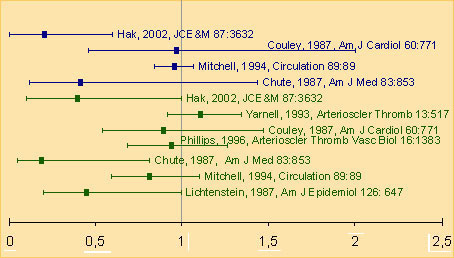
Wenn Bodybuilder nach langjähriger missbräuchlicher Einnahme hoher Dosen anaboler Steroide einen plötzlichen Herztod sterben — oder zumindest kurz davor stehen —, finden sich immer wieder Stimmen, die das als Beweis dafür werten, dass sich Androgene schädigend auf das Herz-Kreislauf-System auswirken. Nun muss man aber sicher nicht erst mühevoll die einschlägigen Daten über Sexualsteroide und kardiovaskuläre Krankheiten aus der wissenschaftlichen Literatur zusammentragen, um zu erkennen, dass Hormon-Abusus nicht mit physiologischen Gegebenheiten zu tun hat. Aber bei kritischer Betrachtung fällt es auch heute noch schwer, die Rolle der Sexualsteroide im Rahmen der kardiovaskulären Gesundheit definitiv zu beurteilen. Eine Fülle kardiovaskulärer Risikofaktoren, die alle direkt oder indirekt von Sexualsteroiden beeinflusst werden, wirken sich auf die Entwicklung von Herz-Kreislauf-Erkrankungen aus. Dennoch kommt eine Auswertung der wichtigsten einschlägigen Studien zu dem Schluss, dass die systemischen endogenen Androgene und Estradiol günstige bzw. neutrale Einflüsse auf die Entwicklung kardiovaskulärer Erkrankungen haben (Muller M, 2003): Physiologisch hohe Androgen-Spiegel senken das
kardiovaskuläre Erkrankungsrisiko
— kardiovaskulärer Benefit ermittelt. Hingegen sind die entsprechenden Ergebnisse für Estradiol bei Männern allenfalls neutral.
Wie lassen sich Sexualhormonwirkungen am
Gefäßsystem erklären?
Testosteron-Effekte führen zur Dilatation der koronaren und herznahen
Gefäße. Hieran sind sowohl Endothel-abhängige als auch
Endothel-unabhängige Mechanismen beteiligt, bei denen nicht näher identifizierte
Rezeptoren für Testosteron auf der Zelloberfläche eine Rolle spielen.
Wahrscheinlich bewirken Androgene ein Öffnen von Kalium-Kanälen in der
Plasmamembran. Über die Plasmamembran-ständigen Rezeptoren werden Effekte
sehr viel rascher ausgelöst als über die klassischen intrazellulären
Androgen-Rezeptoren. Zudem gibt es Befunde, wonach Testosteron durch
Kalzium-antagonistische vasodilatorisch wirkt.
Antiatherogene Effekte könnten dem Testosteron auch insofern zukommen,
als es in Endothelzellen teilweise in Estradiol umgewandelt wird. Dadurch erreichen
die intrazellulären Estradiol-Konzentrationen unter Umständen Spiegel, die
weit oberhalb des systemischen Estradiol-Spiegels liegen. Letzterer hat beim
Mann keinen Einfluss auf die Entwicklung bzw. Verhinderung kardiovaskulärer
Erkrankungen.
Endothelzellen enthalten auch Plasmamembran-ständige Rezeptoren für DHEA.
Über sie wird die Produktion von Stickstoffmonoxid stimuliert. Das nitrose
Gas wirkt als Vasodilatator.
|
|||
| Muller M, van der Schouw YT,
Thijssen JHH, Grobbee DE.
2003. Endogenous sex hormones and cardiovascular disease in men.
J Clin Endocrinol Metab 88:5076-5086. |
|||
|
|||