Organspezifische Androgenität
Androgeneffekte spielen in der Prostata in mannigfaltiger Hinsicht (Entwicklung, Wachstum, Funktion) eine wichtige Rolle.
Sie sind jedoch in erster Linie ein Phänomen des intraprostatischen Androgenstoffwechsels – weitgehend unabhängig vom
Serum-
Androgenität der Prostata von Testosteronmetabolisierung abhängig
- Im Prostatagewebe ist nicht Testosteron sondern sein Metabolit Dihydrotestosteron (DHT) das vorherrschende
Androgen und bevorzugter Reaktionspartner für den
Androgenrezeptor (AR). Aufgrund
unterschiedlicher Geschwindigkeitskonstanten ist der DHT-AR-
In der menschlichen Prostata wird das Enzym 5α-Reduktase Typ II in hohem Maße exprimiert. Durch seine Aktivität wird intraprostatisch eine hohe DHT-Konzentration aufrechterhalten. Diese ist ca. zehnfach größer als der DHT-Spiegel im Serum und gleichfalls um den Faktor 10 höher als die intraprostatische Testosteronkonzentration.
Das in der Prostata wirksame DHT wird weitestgehend lokal durch Reduktion von Testosteron gebildet.
An gesunden Probanden, die sich einer Behandlung mit transdermalem DHT oder Placebo unterzogen, wurde getestet, inwieweit
ein supraphysiologisch erhöhter Spiegel an Serum-DHT die intraprostatische DHT-Konzentration beeinflusst. Dabei ergab
sich kein signifikant erhöhter Spiegel an intraprostatischem DHT wie auch keine veränderte Expression Androgen-
-
Zur Bestimmung der Androgenspiegel im Prostatagewebe stehen gegenwärtig zwar keine handelsüblichen Tests zur Verfügung,
doch die Radioimmunassays, wie sie zur Bestimmung von Androgenen im Serum verwendet werden, sind hierfür nach Gewebeextraktion
prinzipiell geeignet. Die in einer Reihe von Studien ermittelten Konzentrationen an Testosteron und DHT in normalen, nicht
behandelten Prostatae reichten von 0,1 bis 2,0 ng/g bzw. von 1,3 bis 9,2 ng/g, wobei die DHT-Konzentration die der
Testosteronkonzentration jeweils um ein Vielfaches übertraf. Aufgrund der großen Streubreite lassen sich absolute
Messwerte aus verschiedenen Studien nur schwer miteinander vergleichen.
Bei Männern mit Late-onset-Hypogonadismus normalisierten sich unter einer Testosteron-
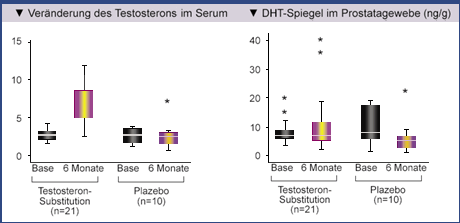
Effekt einer Testosteron-Substitutionstherapie bei Männern mit Late-onset-Hypogonadismus auf
die Konzentrationen von Dihydrotestosteron (DHT) im Prostatagewebe:
Bei Männern mit Late-onset-Hypogonadismus normalisieren sich unter einer Testosteron-Substitutionstherapie zwar die
Serum-
-
Prostata-spezifisches Antigen ist ein Glykoprotein das als (chymo)trypsin-
In der Zirkulation kommt dem PSA keine physiologische Funktion zu. Sein Vorkommen im Serum steht im Zusammenhang mit
benignen oder malignen Krankheitsprozessen in der Prostata. Die Bildung von PSA ist zwar Androgen-abhängig, doch es besteht
andererseits keine signifikante Korrelation zwischen Serum-
-
Bei der Progression von BPH spielen chronische Entzündung und gestörte Immunregulation eine wichtige Rolle.
Die Infiltration der Prostata mit chronisch aktivierten CD4+-T-Lymphozyten und die Sekretion inflammatorischer
Zytokine gelten als bestimmender Faktor in der BPH-Pathogenese. Im Tierversuch führt ein durch Ernährung
mit viel Fett hervorgerufener Hypogonadismus zu histologischen Veränderungen in der Prostata, die durch
Entzündungsrektionen in Verbindung mit gestörten stromalen Strukturen und Hypoxie gekennzeichnet sind.
Dieser Zustand wird durch Testosteronausgleich vollständig normalisiert [4].
In diesem Zusammenhang wurde untersucht, ob bei Männern eine Verbindung von Hypogonadismus zur Schwere der
Entzündung bei BPH besteht, und welchen Effekt der selektive Androgenrezeptor (AR)-Agonist DHT auf
Stromazellen der Prostata ausübt, die von BPH-Patienten nach Prostataresektion in Kultur gehalten wurden.
Der inflammatorische Score war bei Männern mit schwerem Hypogonadismus (Testosteronspiegel deutlich höher als bei
Männern lediglich mit mäßig erniedrigtem Testosteronspiegel.
In prostatischen Stromazellen hat DHT eine immunregulatorische Funktion, indem es deren Fähigkeit
hemmt, Autoimmun- und entzündliche Reaktionen auszulösen
[5].
Tierexperimentelle Daten lassen auf einen Androgen-regulierten Mechanismus schließen, der zur Entwicklung
inflammatorischer Prozesse in der Prostata beitragen kann.
Es wird angenommen, dass Tight Junctions (Zonulae occludentes) im Drüsenepithel der Prostata als Diffusionsbarriere
gegenüber Entzündungsprozessen fungieren. Diese Zellhaften bilden
im Prostataepithel einen Verschlussmechanismus im apikolateralen Bereich der Drüsenzellen aus.
An einem Mausmodell ließ sich nachweisen, dass niedrige Serum-
[1] Page ST, Lin DW, Mostaghel EA, et al. 2011. Dihydrotestosterone administration does not increase intraprostatic androgen concentration or alter prostate androgen action in healthy men: a randomized-controlled trial. J Clin Endocrinol Metab 96:430-437.
[2] Marks LS, Mazer NA, Mostaghel EA, 2006. Effect of testosterone replacement therapy on prostate tissue in men with late-onset hypogonadism. JAMA 296:2351-2361.
[3] Grober ED, Lamb DJ, Khera M, et al. 2008. Correlation between simultaneous PSA and serum testosterone concentrations among eugonadal, untreated hypogonadal and hypogonadal men receiving testosterone replacement therapy. Int J Impot Res 20:561-565.
[4] Vignozzi L, Morelli A, Sarchielli E, et al. 2012b. Testosterone protects from metabolic syndrome-associated prostate inflammation: an experimental study in rabbit. J Endocrinol 212:71-84.
[5] Vignozzi L, Cellai I, Santi R, et al. 2012. Antiinflammatory effect of androgen receptor activation in human benign prostatic hyperplasia cells. J Endocrinol 214:31-43.
[6] Meng J, Mostaghel EA, Vakar-Lopez F, et al. 2011. Testosterone regulates tight junction proteins and influences prostatic autoimmune responses. Horm Cancer 2011:145-156.
| November 2012 | Autor: jfs |
