
Sind die Vorläuferzellen der meisten Hodenkarzinome pluripotent?
Vor mehr als 30 Jahren wurde das testikuläre Carcinoma in situ (CIS) erstmals beschrieben. Schon bald
darauf gab es Anhaltspunkte dafür, daß diese Vorläuferzellen der meisten Hodentumoren fötalen Ursprungs sein
könnten. Mit Hilfe modernster Untersuchungsmethoden wie insbesondere den DNA-Microarrays kam man in jüngster
Zeit zu Ergebnissen, die die Abstammung des testikulären CIS von primordialen Keimzellen oder frühen Gonozyten
nahelegen. Zudem wurden vermehrt Gemeinsamkeiten des Phänotyps von CIS mit dem von embryonalen Stammzellen
deutlich. Darüber hinaus weist das testikuläre CIS eine Reihe von Merkmalen auf, wie sie den hypothetischen
Krebsstammzellen zugeschrieben werden, mit der Besonderheit, pluripotent zu sein [1, 2].
Zellen des präinvasiven CIS haben die Fähigkeit, sich in zahlreiche somatische Tumortypen zu differenzieren
-
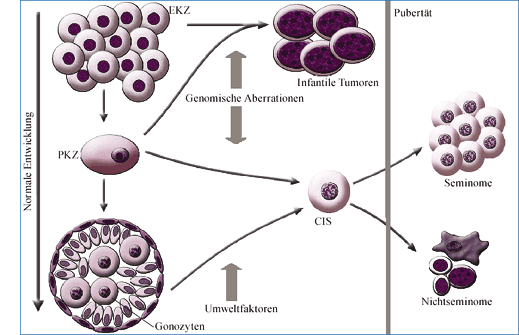
Das Carcinoma in situ (CIS) gilt anerkanntermaßen als der gemeinsame Vorläufer nahezu aller testikulärer
Keimzelltumoren bei Adoleszenten und jungen Erwachsenen. Aus CIS-Zellen können entweder Seminome oder
Nichtseminome entstehen. Beide Keimzelltumoren treten etwa gleich häufig auf. Während die Seminome einen
keimzellartigen Phänotyp beibehalten, bewahren die Nichtseminome verschiedene Merkmale embryonaler
Stammzellen. Zu den Nichtseminomen zählen die embryonalen Karzinome, unterschiedliche Zusammensetzungen
differenzierter teratomatöser Gewebsbestandteile und Dottersacktumoren.
CIS-Zellen befinden sich innerhalb der Hodentubuli entlang der Basalmembran. Sie sind größer als normale
Spermatogonien und fallen durch unregelmäßig geformte Zellkerne mit grobkörnigem Chromatin auf. In Tubuli
mit CIS finden sich darüber hinaus nur noch Sertoli-Zellen.
-
Plazentare alkalische Phosphatase ist ein klassischer Marker für primordiale Gonozyten und wird auch
in CIS exprimiert, so daß das Enzym rutinemäßig zu dessen histochemischen Nachweis genutzt wird.
In embryonalen Stammzellen werden zwei Gene für Transkriptionsfaktoren (POU5F1 und NANOG) exprimiert,
deren Funktion für die Pluripotenz und die Fähigkeit zur Selbsterneuerung bekanntermaßen unentbehrlich
sind. Beide Transkriptionsfaktoren werden auch in testikulären CIS-Zellen exprimiert [3]. Diese Gemeinsamkeit
von CIS mit embryonalen Stammzellen ist wohl das kräftigste Indiz zur Bestätigung der Hypothese, wonach
CIS-Zellen sehr frühen fötalen Ursprungs sind.
-
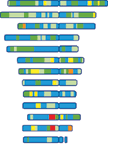
Der Genotyp von CIS-Zellen ist durch chromosomale Verluste und in höherem Maße durch chromosomale
Zugewinne charakterisiert, so daß ein mittlerer Ploidiegrad von 1,5 vorgefunden wird. Involviert
sind insbesondere 17q und 12p. Die Zugewinne von 12p häufig in Form eines Isochromosoms scheinen
mit dem Erlangen invasiven Potentials verbunden zu sein.
In einer aktuellen Untersuchung wurden auf 12p nicht weniger als 73 Gene identifiziert, die in
Keimzelltumoren überexprimiert werden. In embryonalen Karzinomen ist die Überexpression mehrerer
Stammzell-
-
In ähnlicher Weise wie gewöhnliche epitheliale Stammzellen abgestorbene ausdifferenzierte, d. h. nicht
mehr teilungsfähige Zellen in einem Epithelverband ersetzen, versorgen Krebsstammzellen den Tumor
ständig mit neuen determinierten Zellen. Solche Krebsstammzellen bilden eine eigenständige Population,
von deren Tochterzellen ein Teil auf Stammzellniveau verharrt, während ein anderer Teil zu determinierten
Vorläuferzellen wird.
Die Besonderheit des testikulären CIS ist seine Abstammung von primordialen Stammzellen/Gonozyten und
damit den einzigen Zellen im Körper, in denen einige der Pluripotenz-bewahrenden Faktoren embryonaler
Stammzellen erhalten bleiben. Durch diese Pluripotenz ist es möglich, daß das testikuläre CIS Vorläufer
sehr verschiedener Keimzelltumoren sein kann.
-
Die Differenzierung primordialer Keimzellen bzw. Gonozyten zu infantilen Spermatogonien beginnt etwa in
der 20. Schwangerschaftswoche und kann sich bis weit in das erste Lebensjahr hinein fortsetzen. Danach
ist die Expression von Markern der primordialen Keimzellen/Gonozyten wie der plazentaren alkalischen
Phosphatase normalerweise herunterreguliert, so daß sie sich im infantilen Keimepithel nicht mehr
nachweisen läßt.
Die Inzidenz von testikulären Keimzelltumoren hat in den letzten Jahrzehnten merklich zugenommen. Es gibt hierbei jedoch deutliche geographische und ethnische Unterschiede, die dafür sprechen, daß ätiologisch sowohl genetische als auch umweltbedingte Risikofaktoren involviert sind.
Der Beginn der neoplastischen Transformation von frühen Keimzellen wird höchstwahrscheinlich in utero
durch Störungen des Mikromilieus im Keimzellbereich ausgelöst. Insbesondere Hormone, aber auch auto-
bzw. parakrine Faktoren sind an der Regulation der Differenzierungsprozesse beteiligt, bei denen es
während einer längeren Periode zur allmählichen Herunterregulierung embryonaler Stammzelleigenschaften
und der Annahme spermatogonaler Funktionen kommt. Während dieser Phase reagiert das Keimepithel sehr
sensitiv auf jede Art von Milieuveränderung, so daß der Entwicklungsprozeß unter Umständen in einigen
Zellen zum Stillstand kommt.
Literatur:
[1]Almstrup K, Sonne SB, Hoei-Hansen CE, et al. 2006.
From embryonic stem cells to testicular germ cell cancer shall we be concerned? Int J Androl 29:211-218.
[2]Almstrup K, Ottensen AM, Sonne SB, et al. 2005.
Genomic and gene expression signature of the pre-invasive testicular carcinoma in situ. Cell Tissue Res 322:159-165.
[3]Almstrup K, Hoei-Hansen CE, Wirkner U, et al. 2004.
Embryonic stem cell-like features of testicular carcinoma in situ revealed by genome-wide gene expression profiling.
Cancer Res 64:4736-4743.
[4]Korkola JE, Houldsworth J, Chadalavada RSV, et al. 2006.
Down-regulation of stem cell genes, including those in a 200-kb gene cluster at 12p13.31, is associated with in vivo
differentiation of human male germ cell tumors. Cancer Res 66:820-827.
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz
