
erektion — ejakulation — penis — hoden — endokrinologie — fertilität — genetische aspekte — aging male — varia
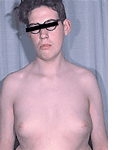
Wachstum der Brustdrüse beim Mann
Im Gegensatz zur Pseudogynäkomastie, die auch als Lipomastie bezeichnet wird, handelt es sich bei der Gynäkomastie nicht um eine rein lokale
Anreicherung von Fettgewebe, wie sie bei Adipositas vorkommt, sondern um eine benigne Vergrößerung der rudimentären männlichen Brustdrüse mit
tastbarem Drüsenkörper. Dem liegt fast immer eine überschießende Estrogenbildung bzw. eine dominierende Estrogenwirkung zugrunde. Die Ursache
dafür sind insbesondere hormonproduzierende Tumoren bzw. eine unzureichende Testosteronwirkung, so dass diesbezüglich zu fahnden ist.
Gynäkomastie nach der Geburt, in der Pubertät und im Alter
-
Bei Neugeborenen ist eine Gynäkomastie als physiologisch anzusehen. Sie wird durch die hohe plazentare Etrogenbildung ausgelöst. Normalerweise
kommt es zur spontanen Rückbildung. In seltenen Fällen kann die Neugeborenen-
Bis zu 60% aller Knaben sind in der Pubertät betroffen. Während der pubertären Übergangsphase werden adrenale Androgene in der Körperperipherie zu Estrogenen konvertiert und führen zur Gynäkomastie, bevor schließlich die testikuläre Testosteronsekretion so hohe Werte erreicht, dass der Androgeneinfluss am Mammagewebe überwiegt. Die männliche Brustentwicklung kann in der Pubertät die Tanner-Stadien 1 und 2 erreichen und bildet sich zumeist innerhalb von zwei bis drei Jahren zurück. Persistiert die Gynäkomastie oder wird ein Tanner-Stadium 3 oder gar 4 erreicht, ist mit einer kompletten Rückbildung nicht zu rechnen, so dass erhebliche psychische Probleme auftreten können und bei Nichtgreifen medikamentöser Maßnahmen sogar eine operative Korrektur erforderlich werden kann.
Auch mit zunehmendem Lebensalter (Endokrinologen, die die Flöhe husten hören, gehen bereits vom 30. Lebensjahr aus) steigt die Ausprägung einer
Gynäkomastie an und kann über 70% der 70-jährigen Männer betreffen. Der altersbedingte Rückgang der Testosteronbildung kann dazu führen, dass die
periphere Estrogenkonversion den Testosteroneinfluss am Mammagewebe soweit antagonisiert, dass es zur Ausprägung einer Gynäkomastie kommt.
-
I. Hypogonadismus: Bei hypogonadalen Männern werden in der Peripherie vermehrt Androgene in Estrogene umgewandelt. Zugleich wird die Estrogenwirkung
infolge einer verminderten Testosteronbildung unzureichend supprimiert. Bedingt durch die erhöhte LH-Sekretion steigt beim hypergonadotropen
Hypogonadismus zudem die Estradiolkonzentration an.
Eine der häufigsten Formen des hypergonadotropen Hypogonadismus ist das Klinefelter-
II. Erhöhte Estrogenbildung: Eine erhöhte Estrogenbildung kommt bei Tumoren der Nebenniere (Adenome, Karzinome), der Hoden (testikuläre Stromazelltumoren,
embryonale Karzinome, Teratokarzinom), der Hypophyse (LH-produzierende Tumoren) sowie im Rahmen paraneoplastischer Syndrome (kleinzellige Leber-,
Bronchial-, Nieren-, Magen- und Pankreaskarzinome) aber auch bei Lymphomen vor. Diese Malignome können zum Teil in erheblichem Ausmaß humanes
Choriongonadotropin (hCG) sezernieren, das dann für die Erhöhung der Estrogenbildung verantwortlich ist.
Mechanismen, die zu einer Steigerung der Aromataseaktivität führen wie z.B. bei einer Hyperthyreose, bedingen eine vermehrte Konversion von adrenalen
Androgenen in Estrogene. Aber auch ein vermehrtes Substratangebot für die Aromatase bei Funktionsstörungen der Nebenniere kann dazu führen. Manche Medikamente
wie Spironolakton und Ketoconazol bewirken, dass weniger Estradiol an SHBG binden kann, und vermehren somit das freie, biologisch aktive Estradiol. Da
Estradiol sowieso in deutlich geringerem Maße an SHBG bindet als Testosteron, wird das Verhältnis von Estradiol zu Testosteron zuungunsten des Testosterons
verschoben.
III. Chronische Erkrankungen, Fehlernährung: Eine häufige Ursache für die Entwicklung einer Gynäkomastie sind chronische Lebererkrankungen mit Übergang
in eine Leberzirrhose, unabhängig davon, ob die Erkrankung viraler Genese ist oder sich auf dem Boden eines Alkoholismus entwickelt hat. Man geht davon
aus, dass in diesen Fällen die Metabolisierung des Estradiols verlangsamt abläuft. Andererseits nimmt die Konzentration an Estrogenen zu, da die
Aromataseaktivität ansteigt. Die Bildung von Androstendion nimmt zu und die des Testosterons ab.
Bei chronischen Nierenerkrankungen, insbesondere bei Patienten mit terminalem Nierenversagen, bildet sich eine Gynäkomastie aus. Bei diesen Patienten findet
sich neben einer erniedrigten Testosteronkonzentration eine erhöhte LH-Konzentration. Darüber hinaus ist die Funktion der Leydig-
Bei Adipositas ist ein Anstieg an Estrogenen, der auf eine erhöhte Aromataseaktivität im Fettgewebe zurückgeführt wird, zu beobachten. Bei Unterernährung nehmen
die LH-, die FSH- und die Testosteronsekretion ab, wohingegen bei einer Gewichtszunahme der FSH-, der LH- und der Testosteronspiegel ansteigen. In erster Linie
kommt es jedoch zu einer erheblichen Steigerung der Estrogenbildung, so dass sich eine Gynäkomastie entwickeln kann.
IV. Medikamente: Exogene Androgene und Anabolika supprimieren sowohl die LH- als auch die FSH-Sekretion und somit die körpereigene Testosteronbildung. Über
einen ähnlichen Mechanismus wirken z.B. das Verapamil und eine Reihe von Psychopharmaka. Auch Opiate hemmen die Gonadotropinsekretion. Sie interferieren mit
den Endorphinen und senken auf der Ebene des Hypothalamus die Freisetzung von Gonadotropin-
Antiandrogene blockieren die Androgenrezeptoren und/oder hemmen die Testosteronbildung. Untersuchungen haben zudem ergeben, dass solche Substanzen die
5alpha-
Spironolakton verdrängt 5alpha-Dihydrotestosteron aus der Rezeptorbindung und setzt vermehrt SHBG-gebundenes Testosteron frei, das sehr rasch metabolisiert
wird, d.h. die metabolische Clearance-Rate steigt an. Spironolakton stimuliert darüber hinaus die Aktivität der Aromatase und steigert die Estrogenbildung.
Demgegenüber hemmen das Ketokonazol und Imidazolderivate – wie auch eine Reihe von Zytostatika – die Testosteronbiosynthese über eine Schädigung
der Leydig-
Hinzuweisen ist auch auf die zumeist akzidentielle Applikation estrogenhaltiger Salben und Lotionen. Dem in manchen Haarwässern enthaltenen 17beta-Estradiol
kommt jedoch keine derartige Wirkung zu, da die Aktivität der 5alpha-Steroidreduktase nur lokal gehemmt wird.
Auch bei Androgenresistenz, konnatalen Defekten der Testosteronbiosynthese und der konnatalen Anorchie entwickelt sich eine Gynäkomastie. Diese Störungen
kommen jedoch wesentlich seltener vor als das Klinefelter-
-
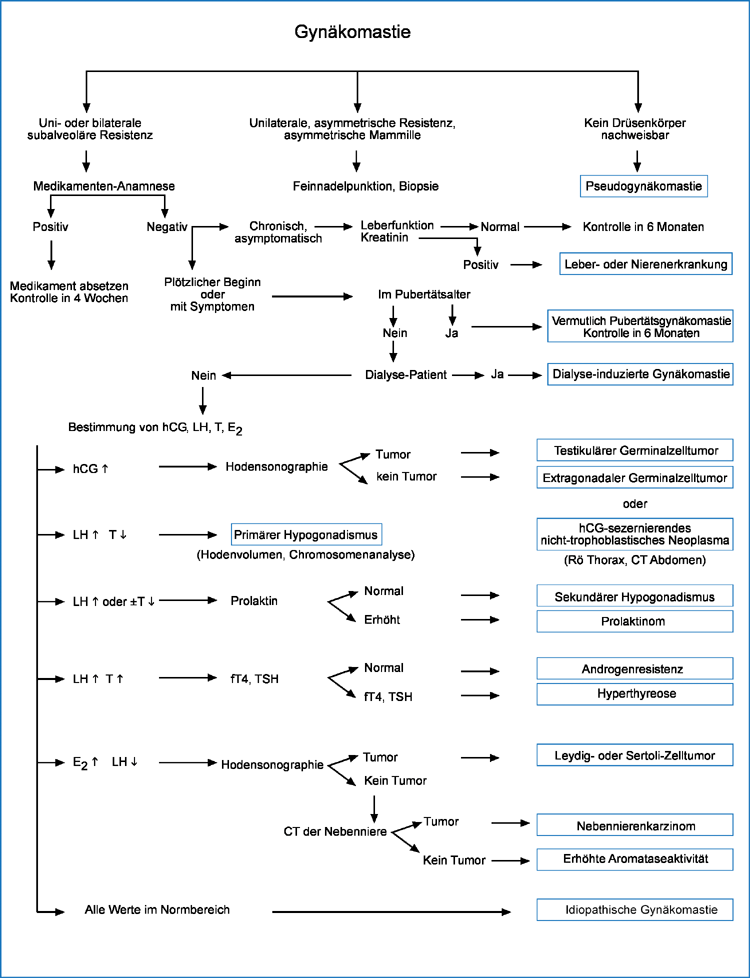
Wichtig ist die Erhebung der Medikamenten-Anamnese. Zu fragen ist nach dem Beginn, der Dauer und der Symptomatik der Mammaveränderungen. Ein akutes Auftreten
mit Schmerzen oder Spannungsgefühl deutet auf eine tumorbedingte Gynäkomastie hin, wohingegen eine asymptomatische, schon länger bestehende Veränderung in der
Regel gutartig ist. Nach Organerkrankungen, Genussmittelkonsum und Tumorerkrankungen ist ebenfalls zu fragen.
Bei der körperlichen Untersuchung sind das Tanner-Stadium bzw. die Mammagröße sowie die Ausprägung der Genital- und Achselbehaarung zu erfassen. Oft lässt
sich palpatorisch kein Drüsenkörper im Mammagewebe nachweisen, trotzdem sollte eine Sonographie zur Beobachtung und Verlaufskontrolle erfolgen. Bei großen
Mammae, Mammillenanomalien oder Resistenzen sollte eine Mammographie durchgeführt werden. Als obligat ist eine Sonographie der Hoden anzusehen, wobei die
Größe zu ermitteln und nach Tumoren zu fahnden ist. Bei Knaben in der Pubertät und unauffälliger Anamnese sind Laboruntersuchungen in der Regel nicht erforderlich.
In anderen Fällen sollte Estradiol, FSH, LH, Testosteron, TSH basal und ggf. SHBG bestimmt werden. Bei Tumorverdacht kommen Bestimmungen von Tumormarkern, hCG
und AFP (Alphafetoprotein) hinzu.
-
Bildet sich eine Pubertätsgynäkomastie nicht zurück, kommt die Gabe von Antiestrogenen oder Aromatasehemmern in Betracht. Aromatasehemmer sollten auch bei
erhöhter Aromataseaktivität angewandt werden. Auf Testolacton in einer Dosierung von 450 mg/die sprechen 90 % der pubertär oder hypogonadal bedingten
Gynäkomastien an.
Naheliegend ist, dass bei medikamentenbedingter Gynäkomastie das auslösende Präparat abgesetzt oder durch ein anderes Medikament ersetzt wird, das keine Gynäkomastie auslöst. Tritt unter der Gabe von Antidepressiva eine Gynäkomastie auf, ist selbstverständlich ein Absetzen nicht möglich und eine Umstellung in manchen Fällen schwierig, weil nicht in allen Fällen ein Alternativpräparat verfügbar ist. Bei tumorbedingter Gynäkomastie ist eine entsprechende Therapie unverzüglich einzuleiten. Bei einer Hyperprolaktinämie, selbst wenn sie durch ein Mikroadenom ausgelöst wird, sollte Bromocriptin oder ein vergleichbares Präparat unter Kontrolle der Prolaktinkonzentration appliziert werden.
Liegt ein Hypogonadismus vor, muss eine Substitution eingeleitet werden, nicht nur wegen der Gynäkomastie, sondern um die Entwicklung schwerwiegender
Komplikationen (Osteoporose) zu verhindern. Bildet sich unter der Substitution die Gynäkomastie nicht zurück, sollten zusätzlich Aromatasehemmer gegeben
werden.
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz
